УГЛЕГРАФИТОВЫХ МАТЕРИАЛОВ
Углеродистые материалы в зависимости от способа получения, исходного сырья могут иметь различную внутреннюю структуру, химические и физические свойства. В природе углеродное вещество существует в трех видах: алмаз, графит, угли.
Алмаз имеет объемноцентрированную кубическую решетку, кокс и многие угли являются аморфными веществами.
Основным структурным элементом графита является двумерная шестиугольная сетка. Она образуется во время графитизации угольных материалов при температурах 2 500...2 700 К и выше.
Атомы в сетках имеют ковалентную связь, сетки располагаются параллельно друг другу и связаны между собой не химической связью, а силами Ван-дер-Ваальса.
Как видно из рис. 35, каждый атом в сетке образует три ковалентные связи, расположенные в одной плоскости, углы между которыми составляют 120 °С. Четвертый валентный электрон не связан, он образует связь типа металлической, хотя подвижность его и ограничена близким расположением шестиугольных сеток. Он-то и обеспечивает графиту многие металлические свойства (электропроводность, теплопроводность). Различные типы связей атомов углерода в сетках и между ними обусловливают пластинчатую структуру графита. Не связанные электроны легко перемещаются в плоскостях, переход в другую плоскость затруднен, отсюда - высокая анизотропия электропроводности.
Расстояние между атомами в сетках (рис. 35, а) равно 1,42 А (0,142 нм), а между сетками (б) - 3,49 А (0,349 нм). Связь между сетками примерно в шесть раз слабее, чем между атомами в сетке.
Следствием такой структуры является высокая температура плавления и испарения, так как трудно вырвать из сетки атом, поскольку это приводит к разрыву ковалентной связи. И наоборот, вследствие непрочной связи между гексагональными сетками, плоскости их легко скользят друг относительно друга, что и объясняет смазочные свойства графита.
К шестиугольным кольцам иногда примыкают атомы и атомные группы линейно полимеризованного графита и других элементов.
На рис. 36 приведена диаграмма агрегатного состояния графита. По оси абсцисс отложена абсолютная температура, а по оси ординат - давление над поверхностью графита в полулогарифмическом масштабе.
|
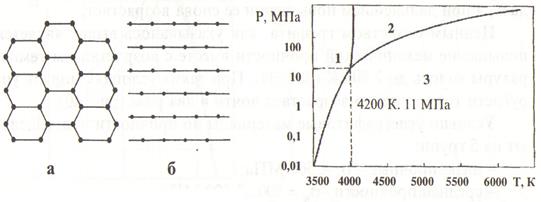
Рис. 35. Структура графита:
а - шестиугольная сетка; б - расположение сеток
Из диаграммы видно, что тройная точка графита соответствует температуре примерно 4 200 К и давлению 11 МПа (110 кгс/см2), то есть, при обычных давлениях он не плавится, а испаряется из твердой фазы, сублимирует. Теплота сублимации равна примерно 170 ккал/моль или 60 000 кДж/кг.
Атомная масса углерода - 12.
Твердость по Моосу: алмаза - 10 ед., графита - параллельно плоскостям - 1,5, в перпендикулярном направлении - 4,5.
Коэффициент термического расширения графита (рис.37) небольшой и при комнатной температуре равен (2...4)Т0'6 (для сравнения, у вольфрама - 8-10"6, у урана - 34Т0"6). Он несколько возрастает с температурой, причем, в разных направлениях отличается примерно в 1,5 раза. От комнатной температуры до 3 300 К графит расширяется не более, чем на 1%.
У разных авторов приведенные свойства могут отличаться, что связано с разными исходными материалами и точностью измерения.
Сравнительно высокая теплоемкость и теплопроводность графита (табл. 17), а также низкий коэффициент термического расширения обусловливают высокую стойкость его при резких тепловых нагружениях (термостойкость).

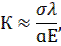
где а - коэффициент термического расширения; 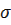 - прочность при растяжении; Е - модуль упругости;
- прочность при растяжении; Е - модуль упругости;  - коэффициент теплопроводности.
- коэффициент теплопроводности.
На рис. 38 представлены графики изменения удельного электросопротивления при повышении температуры. Этот показатель при повышении температуры от комнатной до 800 К слегка падает, а при дальнейшем повышении ее снова возрастает.
Ценным свойством графита, как указывалось выше, является повышение механической прочности вместе с возрастанием температуры вплоть до 2 700 К (рис. 39). При таких условиях модуль упругости тоже линейно возрастает почти в два раза (рис. 40).
Условно углеграфитовые материалы по прочности подразделяют на 5 групп:
- низкопрочные - σв < 500 МПа;
- средней прочности -σв = 500...2 500 МПа;
- высокопрочные - σв > 2000 МПа;
- низкомодульные - Е < 2,5 105 МПа;
- высокомодульные - Е > 2,5 106 МПа.
Нужно отметить, что и прочность, и модуль упругости возрастают с повышением плотности углематериалов.
Как было указано выше, природные углеродные материалы имеют две кристаллические структуры:
- кубическая гранецентрированная или трехмерная сетка (алмаз);
-двумерные плоские сетки, связанные между собой силами Ван-
дер-Ваальса.
В 1992 г. академик И. Е. Вольпин в Вестнике РАН, № 10 сообщил, что еще в 60-е годы были синтезированы две новые кристаллические структуры углерода: карбин и фуллерены. Работы по ним были закрыты.
|
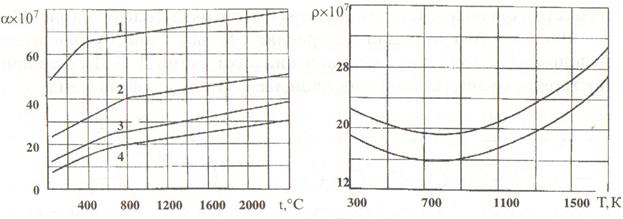
Рис. 37. Зависимости коэффициента
Дата добавления: 2015-07-10; просмотров: 1289;
