Идентификация анионов
Анионы обычно классифицируют по растворимости солей, либо по окислительно-восстановительным свойствам.Так многие анионы (SO 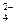 , SO
, SO 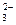 , СO
, СO 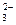 , SiO
, SiO 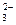 ,PO
,PO 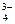 ,F
,F 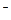 , CrO
, CrO 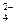 и др.) имеют групповой реагент BaCl2 в нейтральной или слабо кислой среде, так как соли бария и эти анионов мало растворимы в воде. Групповым реагентом в растворе HNO3 на ионы Cl
и др.) имеют групповой реагент BaCl2 в нейтральной или слабо кислой среде, так как соли бария и эти анионов мало растворимы в воде. Групповым реагентом в растворе HNO3 на ионы Cl 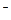 ,Br
,Br 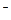 ,I
,I 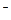 ,SCN
,SCN 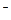 ,СN
,СN 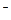 ,S
,S 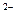 , ClO
, ClO 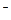 ,[Fe(CN)6]
,[Fe(CN)6] 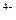 и др. служит AgNO3. Классификация анионов по окислительно-восстановительным свойствам приведена в таблице.
и др. служит AgNO3. Классификация анионов по окислительно-восстановительным свойствам приведена в таблице.
Таблица 18.2 - Классификация анионов по окислительно-восстановительным свойствам
| Групповой реагент | Анионы | Групповой признак |
| KMnO4+H2SO4 I2,крахмал+H2SO4 KI+H2SO4+(крахмал) MnCl2+HCl (конц.) | В о с с т а н о в и т е л и
Cl 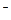 , Br , Br 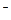 ,I ,I 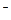 ,SCN ,SCN 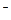 C2O
C2O 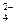 ,S ,S 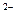 ,SO ,SO 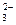 ,NO ,NO 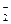 S
S 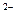 ,SO ,SO 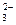 , S2O , S2O 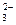 О к с л и т е л и
CrO
О к с л и т е л и
CrO 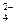 ,MnO ,MnO 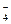 ,ClO ,ClO 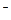 ClO
ClO 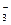 ,NO ,NO 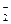 ,BrO ,BrO 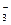 NO
NO 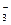 , CrO , CrO 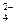 , NO , NO 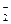 , ClO , ClO 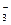 [Fe(CN)6]
[Fe(CN)6] 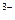 , ClO , ClO 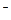 , MnO , MnO 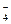 И н е р т н ы е
СO
И н е р т н ы е
СO 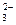 ,SO ,SO 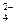 ,SiO ,SiO 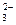 ,PO ,PO 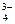 ,F ,F 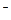 ,BO ,BO 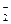
| Обесцвечивание раствора Обесцвечивание раствора Окрашивание раствора Окрашивание раствора |
Анионы можно обнаружить дробным анализом. Для этого групповой реагент ступенчато приливают к анализируемому раствору, первым выпадают в осадок соединения с наименьшими значениями ПР. Отдельные ионы могут быть обнаружены с помощью тех или иных специфических реакций или реагентов. Например, при воздействии на анионы СО 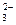 кислотой протекает реакция с выделением пузырьков диоксида углерода:
кислотой протекает реакция с выделением пузырьков диоксида углерода:
СО 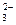 +2Н
+2Н 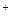
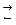 Н2СО3
Н2СО3 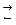 Н2О+СО2
Н2О+СО2
Как и для катионов, имеются реагенты на те или иные анионы(таблица18.2)
Таким образом, химическая идентификация вещества базируется в основном на реакциях осаждения, комплексообразования, окисления и восстановления, нейтрализации, при которых происходит выпадение белого или окрашенного осадка, изменение цвета раствора или выделение газообразных веществ.
Дата добавления: 2015-08-08; просмотров: 1444;
