У аллостерических ферментов особые свойства
Аллостерические ферменты обладают рядом свойств, которые отличают их от не аллостерических. Следует подчеркнуть, что приведенные ниже свойства не обязательны для всех аллостерических белков. Это – общие особенности, по крайней мере некоторые из них проявляются у отдельных аллостерических белков.
- Полимерная структура
- Сигмоидная ( в отличие от гиперболической для не аллостерических) форма кривой зависимости скорости реакции от концентрация субстрата
- Существование эффекторов
- Двухфазный ответ на конкурентные ингибиторы
- Потеря аллостерических свойств при денатурации
Полимерная структура. Все аллостерические ферменты и белки имеют полимерную или четверичную структуру. Это значит, что типичный аллостерический белок будет состоять из ряда отдельных белковых цепей или субъединиц, которые связаны друг с другом слабыми взаимодействиями типа водородных связей и гидрофобного взаимодействия. Полимерная структура – ключевое свойство для функции аллостерического белка.
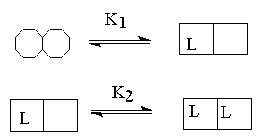
| 
|
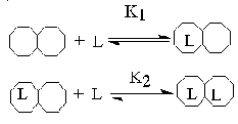
| Кооперативное связывание | Не кооперативное связывание |
Аллостерический фермент содержит ряд активных центров, в самом простом случае по одному на субъединицу, каждый из которых может связываться с лигандом. Взаимодействие между этими центрами и является основой кооперативности. Так, в типичном аллостерическом ферменте связывание молекулы лиганда к одному из активных центров инициирует изменение конформации, которое увеличит способность других активных центров связывать лиганды (положительная кооперативность. K2 << K1) или понизит их сродство к лиганду (отрицательная кооперативность K1 << K2). При отсутствии кооперативного взаимодействия -K1 = K2.
Субъединицы связаны друг с другом слабым взаимодействием, поэтому аллостерический фермент будет часто существовать в растворе в равновесии между целым ферментом и индивидуальными субъединицами. При большом числе субъединиц могут возникать промежуточные формы между этими крайними формами, в которых будут связаны несколько субъединиц, но в меньшем количестве, чем в целом ферменте. В этом случае одиночная субъединица не может быть каталитически активна. Самая маленькая каталитически активная структура названа протомером. Связывание лигандов (субстрат, продукт или эффектор) к ферменту изменяет позицию равновесия между субъединицами.
Сигмоидная кинетика. При составлении графика зависимости скорости от концентрации субстрата для ферментативной реакции для аллостерических ферментов получается несколько иной тип кривой, называемой сиг  моидальной в отличие от гиперболической для не аллостерических ферментов. Ключевой элемент этой кривой, который отличает ее от гиперболической - «носок» у основания кривой , который можно видеть при низких концентрациях субстрата. В этой точке увеличение концентрации субстрата вызывает очень незначительное увеличение в скорости - диаграмма имеет очень небольшой наклон. При более высоких уровнях субстрата, (выше 0.5 единиц концентрации на этом графике) можно видеть, что увеличение концентрации субстрата начинает вызывать намного более значительное увеличение в скорости, и кривая становится более крутой. При высоких концентрациях субстрата график становится очень похожим на гиперболический график, и можно видеть такую же пологую кривую как и на графике уравнения Михаэлиса и Ментен.
моидальной в отличие от гиперболической для не аллостерических ферментов. Ключевой элемент этой кривой, который отличает ее от гиперболической - «носок» у основания кривой , который можно видеть при низких концентрациях субстрата. В этой точке увеличение концентрации субстрата вызывает очень незначительное увеличение в скорости - диаграмма имеет очень небольшой наклон. При более высоких уровнях субстрата, (выше 0.5 единиц концентрации на этом графике) можно видеть, что увеличение концентрации субстрата начинает вызывать намного более значительное увеличение в скорости, и кривая становится более крутой. При высоких концентрациях субстрата график становится очень похожим на гиперболический график, и можно видеть такую же пологую кривую как и на графике уравнения Михаэлиса и Ментен.
Такой тип диаграммы характерен для положительной субстратной кооперативности. При очень низких концентрациях субстрата лишь небольшое количество активных центров фермента связываются с субстратом и фермент будет иметь низкое сродство к субстрату. Поэтому добавление большего количества субстрата вызывает только небольшое увеличение в скорости реакции, поскольку субстраты связываются очень плохо. Однако, по мере повышения числа связавшихся молекул субстрата, положительный кооперативный эффект увеличивает способность фермента связывать субстраты, и кривая на графике начинает это показывать, круто перемещаясь вверх. В конечном счете, точно так же как и в случае классической гиперболической кривой, ферменты постепенно насыщаются субстратом и линия делается пологой, показывая достижение максимальной скорости. Такой тип кривой не обязателен для всех аллостерических ферментов. В частности, многие ферменты катализируют превращение нескольких субстратов и исследования показывают, что такие ферменты могут проявлять положительную кооперативность (сигмоидальная кривая) для одного субстрата и катализировать реакцию по гиперболической кривой для другого.
Эффектор.Аллостерические ингибиторы и активаторы объединяют общим названием эффекторы. Эффектор - одна из важных особенностей аллостерических ферментов. Возможность изменять скорость реакции, катализируемой ферментом, ингибиторами и активаторами - краеугольный камень принципов регуляции метаболизма. Следующий график показывает пути, по которым эффекторы изменяют кинетический график типичного аллостерического фермента с положительной субстратной кооперативностью.
 Центральная линия графика - типичная сигмовидная кривая в отсутствии любого эффектора. В присутствии активатора (А) скорость реакции повышается при любой данной концентрации субстрата, в то время как ингибитор уменьшает скорость реакции. Интересны и изменения общей формы кривой по сравнению с центральной линией. Ингибитор увеличил сигмовидную форму, удлиняя «носок» кривой, в то время как активатор оказывал противоположный эффект. При более высокой концентрации активатора график в целом приобретает характер гиперболы. Это указывает на то, что аллостерический ингибитор увеличивает уровень субстратной кооперативности, в то время как активатор уменьшает его.
Центральная линия графика - типичная сигмовидная кривая в отсутствии любого эффектора. В присутствии активатора (А) скорость реакции повышается при любой данной концентрации субстрата, в то время как ингибитор уменьшает скорость реакции. Интересны и изменения общей формы кривой по сравнению с центральной линией. Ингибитор увеличил сигмовидную форму, удлиняя «носок» кривой, в то время как активатор оказывал противоположный эффект. При более высокой концентрации активатора график в целом приобретает характер гиперболы. Это указывает на то, что аллостерический ингибитор увеличивает уровень субстратной кооперативности, в то время как активатор уменьшает его.
K-системы и V-системыКак видно из графика все линии стремятся к одному значению Vmax, но при этом эффектор влияет на связывание субстрата, что отмечено в изменении Км. Такая ситуация названа K-системой. Некоторые ферменты имеют эффекторы, которые изменяют Vmax. Тогда говорят о V-системе..
Двухфазный ответ на конкурентные ингибиторы. Помимо взаимодействия с эффекторами, аллостерические ферменты являются объектом обычного конкурентного торможения, подобно любому другому ферменту. Классические конкурентные ингибиторы действуют, потому что они структурно подобны субстрату фермента. В аллостерическом ферменте, с положительной субстратной кооперативностью конкурентный ингибитор также достаточно близок по строению субстрату, мог бы иметь те же самые свойства кооперативности как и субстрат. В этом случае, низкая концентрация конкурентного ингибитора увеличивает способность фермента связывать молекулы субстрата, что фактически равно увеличению скорости реакции. При более высоких концентрациях ингибитора это блокировало бы связывание субстрата обычным способом, и реакция замедлится. Ингибитор тем самым оказывает двухфазный эффект. При низких концентрациях - он действует как активатор, в то время как при высоких концентрациях, он действует как ингибитор.
Денатурирующие агенты.Денатурация – нарушение пространственной структуры фермента с последующей потерей активности фермента. Денатурация вызывается рядом факторов, включая высокую температуру, экстремальные значения рН и химические денатурирующие реактивы типа мочевины.
Аллостерические ферменты, подвергнутые умеренному воздействию одним из этих факторов денатурации часто вначале теряют свои аллостеричесие свойства (субстратную кооперативность) при сохранении способности катализировать реакции. Это хорошее доказательство того, что третичная структура играет ведущую роль не только для механизмов катализа, но для механизмов аллостерической регуляции.
Дата добавления: 2015-06-27; просмотров: 1713;
