Изучение свойств известковых вяжущих. Стандарты
Определение суммарного содержания активных оксидов кальция и магния в кальциевой извести. В соответствии с ГОСТ 22688-77, для определения суммарного содержания оксидов кальция и магния в негашеной и гидратной кальциевой извести используется метод титрования, основанный на реакции нейтрализации извести соляной кислотой.
Навеску извести массой 1 г помещают в коническую колбу вместимостью 250 мл, наливают 150 мл дистиллированной воды, закрывают стеклянной воронкой или часовым стеклом и нагревают 5-7 мин до температуры кипения. Раствор охлаждают до температуры 20-30°С, промывают стенки колбы и стеклянную воронку (или часовое стекло) кипяченой дистиллированной водой, добавляют 2-3 капли 1%-ного спиртового раствора фенолфталеина и титруют при постоянном взбалтывании 1 н раствором соляной кислоты до полного обесцвечивания раствора. Титрование считают законченным, если в течение 8 мин при периодическом взбалтывании раствор останется бесцветным.
Титрование следует производить медленно, добавляя кислоту по каплям.
Содержание активных оксидов кальция и магния А, %, для негашеной извести вычисляют по формуле
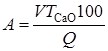 ,
,
где V - объем раствора 1 н соляной кислоты, пошедший на титрование, мл; ТСаО - титр 1 н раствора соляной кислоты, выраженный в СаО (ТСаО = 0,02804 г), г; Q - масса навески извести, г.
Содержание активных оксидов кальция и магния А, %, для гидратной извести вычисляют по формуле
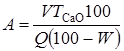 ,
,
где W - влажность гидратной извести, %.
Для определения титра 1 н раствора соляной кислоты, выраженного в СаО, навеску около 1 г углекислого натрия, предварительно высушенного до постоянной массы при температуре 250-270°С, помещают в коническую колбу вместимостью 250 мл и растворяют дистиллированной водой до 80-100 мл.
Полученный раствор титруют устанавливаемым 1 н раствором соляной кислоты в присутствии метилового оранжевого индикатора до перехода желтой окраски раствора в оранжево-розовую.
Титр 1 н раствора соляной кислоты, выраженный в СаО (ТСаО), г, вычисляют по формуле
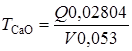 ,
,
где Q - масса навески углекислого натрия, г; V - объем 1 н раствора соляной кислоты, пошедшей на титрование, мл; 0,053 - количество натрия углекислого, соответствующее 1 мл точно 1 н раствора соляной кислоты, г.
Определение суммарного содержания активных оксидов кальция и магния в магнезиальной, доломитовой и гидравлической извести. Содержание активного оксида кальция определяется сахаратным способом. Навеску извести массой не более 0,25 г помещают в коническую колбу вместимостью 500 мл, добавляют 50 мл раствора сахарозы и энергично взбалтывают в течение 15 мин. Затем прибавляют 2-3 капли фенолфталеина и титруют 1 н раствором соляной кислоты. Титрование производят по каплям до первого исчезновения розовой окраски. Количество активного оксида кальция А1, %, вычисляют по формуле
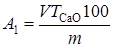 ,
,
где V - объем 1 н раствора соляной кислоты, пошедший на титрование, мл; ТСаО - титр 1 н раствора соляной кислоты, выраженный в СаО (ТСаО = 0,02804 г), г; т - масса навески извести, г.
Содержание активного оксида магния определяют трилонометрическим методом. Массу навески извести не более 0,5 г помещают в стакан вместимостью 200-250 мл, смачивают ее водой и прибавляют 30 мл 1 н соляной кислоты. Стакан закрывают часовым стеклом и нагревают в течение 8-10 мин до температуры кипения, затем часовое стекло ополаскивают дистиллированной водой и после охлаждения раствор переливают в мерную колбу вместимостью 250 мл, доливают дистиллированной водой до метки и тщательно перемешивают. После отстаивания раствора отбирают пипеткой 50 мл, переносят в коническую колбу вместимостью 250 мл и добавляют 50 мл дистиллированной воды, 5-10 мл аммиачного буферного раствора, 5-7 капель кислотного хром темно-синего индикатора и титруют при сильном взбалтывании 0,1 н раствором трилона Б до перехода красной окраски раствора в сине-зеленую или синюю.
По окончании титрования отмечают объем V1 израсходованного трилона Б в миллилитрах.
Из этой же мерной колбы отбирают 25 мл раствора в коническую колбу вместимостью 250 мл, приливают 100 мл дистиллированной воды и перемешивают. Затем добавляют 3 мл триэтаноламина, 25 мл 20%-ного раствора NaOH и вновь перемешивают. Через 1-2 мин добавляют на кончике шпателя флуорексон и титруют раствором трилона Б до перехода флуоресцирующей розово-зеленой окраски раствора в устойчивую розовую при наблюдении на черном фоне. Отмечают объем V2 израсходованного раствора трилона Б в миллилитрах.
Содержание активного оксида магния А2, %, вычисляют по формуле
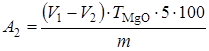 ,
,
где V1 - объем 0,1 н раствора трилона Б, пошедший на титрование СаО + MgO, мл; V2 - объем 0,1 н раствора трилона Б, пошедший на титрование СаО, мл; ТMgO - титр 0,1 н раствора трилона Б, выраженный в MgO (ТMgO = 0,002015 г), г; 5 - коэффициент, учитывающий определение MgO в аликвотной части раствора; т - масса навески извести, г.
Содержание активных оксидов кальция и магния А, %, определяется суммой величин А1 + А2.
Для установки титра трилона Б приливают из бюретки 20 мл 0,1 н раствора сернокислого магния, приготовленного из фиксанала, в коническую колбу вместимостью 250-300 мл, разбавляют раствор до 100 мл водой, нагревают до 60-70°С, приливают 15 мл аммиачного буферного раствора и 5-7 капель кислотного хром темно-синего индикатора и титруют 0,1 н раствором Б при интенсивном помешивании до перехода красной окраски раствора в устойчивую сине-сиреневую или синюю с зеленоватым оттенком.
Титр 0,1 н раствора трилона Б ТMgO, выраженный в MgO, г, вычисляют по формуле
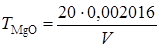 ,
,
где 0,002016 - количество оксида магния, соответствующее 1 мл точно 0,1 н раствора трилона Б, г; V - объем 0,1 н раствора трилона Б, пошедший на титрование 20 мл 0,1 н раствора сернокислого магния, мл.
Определение содержания СО2 в извести. Содержание СО2 в извести можно определить весовым методом и на кальциметре газообъемным методом (экспресс-методом).
В е с о в о й м е т о д. Тигель с навеской извести, прокаленной при температуре 520 ± 10°С, помещают на 1 ч в муфельную печь, нагретую до температуры 975 ± 25°С. После охлаждения тигля с навеской в эксикаторе производят взвешивание.
Содержание СО2, %, вычисляют по формуле
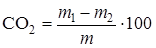 ,
,
где т1 - масса навески после прокаливания при 520°С; т2 - масса навески после прокаливания при 975°С; т - масса навески извести, г.
Г а з о о б ъ е м н ы й м е т о д. Газообъемный метод основан на измерении выделившегося углекислого газа в результате воздействия соляной кислоты на карбонаты кальция и магния. Определение содержания СО2 в извести производится при помощи кальциметра (рис. 2.17).
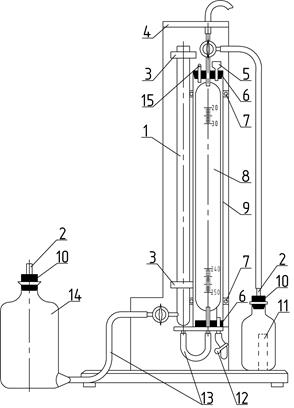
Рис. 2.17. Кальциметр:
1 - цилиндр с краном; 2 - отводная трубка; 3 - клеммы
для цилиндра; 4 - подставка; 5 - воронка; 6 - резиновая пробка
к мантии; 7 - клемма для мантии; 8- бюретка с краном;
9 - мантия; 10 - резиновая пробка; 11 - склянка с пробиркой;
12 - пружинный зажим; 13 - соединительная резиновая трубка;
14 - склянка с тубусом; 15 - отверстие для термометра
Перед началом работы определяют герметичность прибора. Склянку с пробиркой 11 закрывают пробкой 10, соединенной резиновой трубкой с бюреткой 8. Кран цилиндра 1 открывают, а кран бюретки переводят в вертикальное положение, соединяя с атмосферой бюретку и склянку с пробиркой. В мантию 9 бюретки наливают воду, а в склянку с тубусом 14 - подкрашенный насыщенный водный раствор хлористого натрия. Путем вертикального перемещения склянки с тубусом доводят уровень жидкости в бюретке до нулевой отметки, кран бюретки устанавливают в горизонтальном положении, перекрывая выход в атмосферу и соединяя бюретку и склянку с пробиркой. Затем уровень жидкости в цилиндре при помощи склянки с тубусом доводят до отметки 120-130 мл (по шкале бюретки), закрывают кран цилиндра и оставляют прибор в таком состоянии на несколько часов. Если уровень жидкости в бюретке изменяется, то необходимо проверить на герметичности все соединительные части: трубки, краны, пробки. Если уровень жидкости не изменился - определяют концентрацию СО2 в извести.
Массу навески извести около 1 г помещают в склянку с пробиркой 11 и при помощи воронки в пробирку наливают около 10 мл
20%-ного раствора соляной кислоты. Склянку с пробиркой 11 закрывают пробкой 10, соединенной резиновой трубкой 2 с бюреткой 8. Во время проведения опыта склянку с пробиркой необходимо брать только за горлышко.
Кран бюретки 8 устанавливают в вертикальное положение, соединяя с атмосферой бюретку и склянку с пробиркой 11. Открывают кран цилиндра 1 и, изменяя высоту положения склянки с тубусом 14, уровень жидкости в цилиндре и бюретке устанавливают на отметке 20 мл. После этого кран цилиндра закрывают, а кран бюретки переводят в горизонтальное положение, перекрывая атмосферу от склянки с пробиркой и бюретки. Для соединения навески с кислотой склянку с пробиркой при открытом кране цилиндра наклоняют и встряхивают. В результате взаимодействия карбонатной составляющей пробы с соляной кислотой выделившийся СО2 попадает в бюретку, вытесняя из нее жидкость в цилиндр и склянку с тубусом. Для охлаждения склянку с содержимым помещают в сосуд с водой, имеющей температуру воды в мантии бюретки. После стабилизации столба жидкости в бюретке, т. е. прекращения выделения СО2, кран цилиндра открывают и уравнивают жидкость в бюретке и цилиндре. При получении одинаковых уровней жидкости по разности уровней до и после реакции по шкале бюретки производят отсчет объема выделившегося СО2. Одновременно замеряют температуру воды в мантии бюретки (температура опыта) и атмосферное давление по барометру.
Содержание СО2, %, вычисляют по формуле
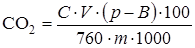 ,
,
где С - масса 1 мл СО2 при температуре и атмосферном давлении опыта, мг (табл. 2.5); V - объем выделившегося СО2, мл; р - атмосферное давление по барометру, мм рт. ст.; В - давление водяных паров при температуре опыта над насыщенным раствором NaCl, мм рт. ст. (табл. 2.6); т - масса навески извести, г.
Таблица 2.5
Масса 1 мл СО2 в зависимости от температуры
Дата добавления: 2015-06-17; просмотров: 3670;
