Смачивание паяемого металла припоем, растекание и затекание его в зазор.
Исходя из определения пайки, как процесса создания неразъемных соединений, можно выделить три стадии взаимодействия жидкой фазы с твердой при образовании физического контакта: смачивание жидким (расплавленным) припоем, растекание и затекание припоя в зазор.
Смачиванием называется первая стадия физико-химического взаимодействия расплавленного припоя с паяемым материалом, проявляющееся в растекании припоя или образовании мениска с конечным краевым углом смачивания. В физическом смысле под смачиванием понимается характер контактного взаимодействия жидкого вещества с твердым, при котором прочность связи их частиц больше, чем между элементарными частицами в жидкости.
В процессе смачивания атомы жидкого металла (припоя) сближаются с атомами паяемой поверхности на расстояние, соизмеримое с расстояниями между атомами в кристаллической решетке (менее 10 ангстрем, 1 Å=1·10–10 м). Атомы припоя, вступившие во взаимодействие с твердым паяемым металлом, при смачивании образуют слой, по которому лежащие над ним слои атомов припоя свободно перемещаются в плоскости параллельной поверхности растекания.
При смачивании две свободные поверхности заменяются одной границей раздела фаз между твердым металлом и расплавом припоя с более низкой свободной поверхностной энергией системы. На этой стадии образования паяного соединения большую роль играют квантовые процессы между частицами атомных размеров. Поскольку при пайке взаимодействие происходит между атомами разнородных металлов, то основную роль играют переходы электронов с внешних сфер атомов.
Интенсивность процессов смачивания определяется характером реакции взаимодействия атомов. Если реакция эндотермическая, то энергия термической активации должна превысить активационный барьер и обеспечивать дополнительную теплоту, необходимую для протекания реакции. При экзотермической реакции после преодоления активационного барьера, теплота, выделяемая в процессе самой реакции, вызывает развитие процесса смачивания.
При смачивании паяемой поверхности твердого тела каплей жидкого припоя условие ее равновесия может быть выражено через векторы сил поверхностного натяжения на границе взаимодействия трех фаз (твердой, жидкой и газообразной).
Поверхностное натяжение – работа обратимого изотермического образования единицы площади этой поверхности (в случае жидкой поверхности раздела можно рассматривать как силу, действующую на единицу длины контура поверхности и стремящуюся сократить поверхность до минимума при заданных объёмах фаз).
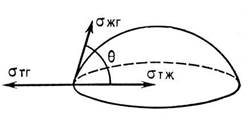
| 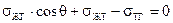 Угол θ называют краевым углом смачивания, откуда:
Угол θ называют краевым углом смачивания, откуда:
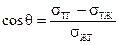 – (уравнение Юнга) – (уравнение Юнга)
|
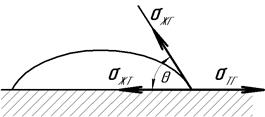
Величину cosθ, характеризующая смачивающую способность жидкости, называют коэффициентом смачивания. Если cosθ>0, а θ<90°, жидкость (припой) смачивает поверхность твердого тела, если cosθ<0, а θ>90°, жидкость практически не смачивает поверхность твердого тела (рис. …).
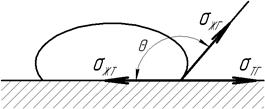
а) б)
Рис. ….Величина краевого угла смачивания:
а – при смачивании подложки, б – при несмачивании подложки.
Анализ уравнения Юнга показывает, что чем больше поверхностное натяжение жидкого припоя, тем хуже он смачивает паяемый металл. Однако, σЖГ не может однозначно характеризовать величину cosθ. Процесс смачивания зависит от соотношения физико-химических свойств взаимодействующих материалов, и, в частности, от свободной энергии паяемого материала, косвенно выраженной через σТГ. Количественная оценка процессов взаимодействия на границе трех контактирующих фаз в настоящее время весьма затруднена, поскольку по величинам σТГ и σЖГ судить о смачивании не представляется возможным.
Движущей силой, приводящей к деформированию капли и увеличению площади межфазной поверхности является уменьшение свободной энергии системы. Этот процесс протекает до минимального энергетического состояния, тогда σТГ–σЖТ можно рассматривать как движущую силу процесса растекания. Из термодинамических расчётов следует, что низкие значения межфазных натяжений (σЖТ) в металлических системах, практически во всех случаях должны обеспечивать полное смачивание. Отсутствие смачивания в подобных системах является следствием наличия промежуточных оксидных или иных прослоек на межфазной границе.
Растекание расплава припоя определяется соотношением сил адгезии (прилипание веществ без их обмена элементарными частицами и электронами по месту их физического контакта, то есть, без их взаимной диффузии) припоя и поверхности паяемого металла и силами связи между частицами припоя (когезии). Работа адгезии определяется в виде разности поверхностных натяжений твердой и жидкой фаз в контакте с газом (σТГ и σЖГ) до контакта между твердой и жидкой фазами и после их контакта, и может быть выражена уравнением Дюпре (1969 г.):
Wa=σТГ+σЖГ–σТЖ,
как изменение свободной энергии системы при переходе ее в новое состояние.
Адгезия и смачивание – это две стороны одного и того же явления, возникающего при контакте жидкости с твердой поверхностью. Адгезия обуславливает взаимодействие между твердым телом и, находящейся с ней в контакте, жидкостью, а смачивание – это явление, которое имеет место в результате этого взаимодействия.
При равновесии системы, например, при рассмотрении капли жидкости на плоской поверхности при постоянной температуре, массе и объеме фаз, свободная энергия системы минимальна, то есть ΔЕ=0. В этом случае растекание жидкости идет по своеобразному механизму «наползания» ее на поверхность твердого тела (рис. …). При смещении периметра смачивания на величину Δх от точки А, поверхность жидкости увеличится на величину:
(Δх+Δz)·dl,
где dl – участок длины периметра смачивания.
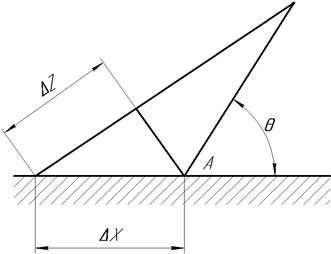
Рис. …. Растекание жидкости при равновесии системы.
Возрастание энергии системы при этом составит:
(Δх+Δz)·dl· σЖГ
Частью новой поверхности Δх·dl жидкость придет в контакт с твердым телом. При этом высвобождается энергия
Δх·dl·Wa
В условиях равновесия системы:
ΔЕ=–(Δх+Δz)·dl· σЖГ+Δх·dl·Wa=0,
поскольку Δz=Δх·cosθ=>
Δх·σЖГ+Δх·cosθ·σЖГ=Δх·Wa=>
Wa=σЖГ · (1+cosθ).
Полное растекание припоя по поверхности паяного изделия происходит при θ=0, тогда cosθ=1, и соответственно σЖГ=σТГ–σТЖ. Подставив эти значения в уравнение работы адгезии, получим, что:
Wa=2σЖГ.
Но при этом работа когезии (сцепление частиц физического тела под действием сил притяжения), будет равна:
WК=2σЖГ
поскольку когезия частиц припоя оценивается работой образования двух поверхностей жидкости при ее разрыве. Следовательно полное растекание наблюдается при Wa=WК, то есть, адгезионная связь заменяется когезионной.
Таким образом, в соответствии с характером взаимодействия веществ смачивание твердого вещества жидким (припоем) может быть трех типов:
1) физическим или обратимым (адгезионная, без обмена атомами или ионами);
2) хемосорбционным (с обменом электронами, приводящим к химической адгезии);
3) физико-химическим, при котором имеют место взаимное растворение или химическая реакция между контактирующими веществами (обмен атомами и электронами, приводящим к когезии).
Условия смачивания в значительной степени зависят от того, в каком состоянии находятся контактирующие твердая и жидкая фазы.
В процессах смачивания различают равновесные и неравновесные системы, отличающиеся друг от друга по характеру взаимодействия.
В равновесных системах контактирующие фазы находятся в условиях термодинамического равновесия, то есть, химические потенциалы компонентов, температура и давление каждой из фаз постоянны. Если эти фазы привести в контакт, образуется поверхность раздела с вполне определенным конечным значением межфазной поверхностной энергии, при система будет оставаться стабильной и равновесной. Переход вещества через межфазную границу отсутствует, и при высоких значениях межфазной энергии и поверхностного натяжения устанавливается вполне определенный конечный краевой угол смачивания не равный нулю. В реальных условиях отклонения от равновесного краевого угла смачивания обусловлено шероховатостью поверхности, ее наклоном и т.п. Межфазная граница и ее энергия в этих условиях зависит только от различия в строении и природы контактирующих фаз, и уменьшается при их сближении.
В неравновесных системах фазы находятся в термическом равновесии, при одинаковом давлении, но не находятся в химическом равновесии (рис. … – фазы а' и b').
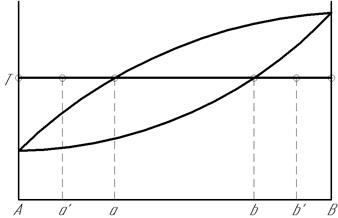
Рис. ….
В этой системе после создания контактной поверхности будут происходить процессы, направленные на достижение химического равновесия, такие как, процессы растворения, переноса компонентов из одной фазы в другую, химические превращения, приводящие систему в равновесное состояние (точки а и b). Межфазная энергия σТЖ такой системы будет изменятся во времени, и будет определяться протекающими в системе на межфазной границе необратимыми процессами химического взаимодействия. Протекание этих процессов является мощным источником снижения межфазного натяжения. Действительно, выделяющаяся при реакции энергия на межфазной границе равна энергии связи, а следовательно приближенно равна работе адгезии (по Дюпре):
Wa=σТГ+σЖГ–σТЖ
или
σТЖ=σТГ+σЖГ–Wa,
отсюда рост энергии связи жидкости и твердого тела Wa, вызывает снижение межфазного натяжения σТЖ. Работу в общем случае можно представить в виде:
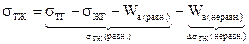
σТЖ=σТЖ.равн.–ΔσТЖ.неравн.
где σТЖ.равн. – является функцией различия природы и свойств контактирующих фаз;
ΔσТЖ.неравн. – является функцией отклонения системы от равновесного состояния.
Следует отметить, что изменение натяжения на границе твердой и жидкой фаз при интенсивном химическом взаимодействии на межфазной границе может быть столь значительным, что ΔσТЖ.неравн>σТЖ.равн. и тогда σТЖ<0, то есть, на границе раздела фаз энергия будет понижаться. Такая система является термодинамически неустойчивой. Однако, в связи с малыми скоростями диффузии, особенно в твердой фазе, оно может сохранятся достаточно длительное время. Зависимость σТЖ, θ и Wа от времени есть характерная особенность неравновесных систем.
Неравновесное растекание. Если в первоначальный момент времени краевой угол смачивания отличен от равновесного, причем θ>θ0, жидкость будет растекаться до тех пор, пока не займет равновесное положение. В точке контакта трех фаз будет приложена сила Fq=σЖГ·(cosθ0–cosθt). Силами, препятствующими растеканию, будут инерция массы жидкости и ее вязкость. Краевой угол смачивания для этого процесса не является равновесным.
Для равновесного процесса растекания изменение межфазной энергии происходит с малой скоростью, так, что жидкость успевает принять равновесную форму, соответствующую значениям σТГ, σЖГ, σТЖ и θ.При этом влиянием сил вязкости и инерции можно пренебречь. Для этого процесса на всех его стадиях справедливо соотношение:
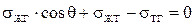
Дата добавления: 2015-01-29; просмотров: 1708;
