Десульфурация
При отвердевании стали в результате избирательной кристаллизации сера, растворенная в расплавленном металле, концентрируется в остающейся жидкости. Обладая очень малой растворимостью в железе, сера выделяется на границах зёрен металла в виде легкоплавких соединений в смеси с оксидами железа. Сталь с повышенным содержанием серы становится красноломкой – хрупкой при температурах горячей обработки (800-1000°С) а в холодном состоянии сталь имеет низкую механическую прочность.
При производстве литейных сплавов сера может находиться в газовой фазе (SO2), в топливе (FeS), в металлическом и шлаковом расплавах. Удалить серу из металла методом окислительного рафинирования невозможно, так как сера обладает меньшим сродством к кислороду, чем железо.
Десульфурация расплавленного металла производится переводом серы в шлак при помощи реагентов, способных давать более прочные и существенно менее растворимые в железе сульфиды, чем FeS, например CaS, MgS, MnS, Na2S и др. В качестве такого реагента чаще всего используют оксид кальция CaO.
В плавильных агрегатах процесс сводится к взаимодействию шлака, содержащего CaO, с металлом по реакции
[FeS]+(CaO)=(FeО)+(CaS),
которая является частным случаем взаимодействия серы, растворенной в железе, с основными оксидами шлака
[FeS]+(МеO)=(FeО)+(МеS).
Константа равновесия
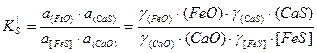 .
.
Концентрации (CaS) и [FeS] можно заменить общим содержанием серы в шлаке (S) и расплаве [S] с введением коэффициентов активности серы в шлаке γ(S) и расплаве γ[S], учитывающих в суммарном виде степень связанности серы в соответствующих фазах. Тогда
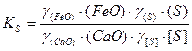 .
.
Коэффициент распределения 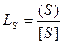 .
.
Эта величина служит для оценки обессеривающей способности шлака.
Из уравнения константы равновесия
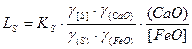 .
.
Отсюда следует, что константа распределения серы LS возрастает с увеличением активности СаО, то есть основности шлака, и со снижением активности FeO, то есть его окислительной способности.
Таким образом, для обессеривания наиболее пригодны основные восстановительные процессы.
В электросталеплавильном процессе после завершения окислительного рафинирования наводят раскислительный шлак с низким содержанием FeO (менее 1%) путём введения восстановителей (C и Si). Это обеспечивает и раскисление и десульфурацию стали.
Обессеривающая способность шлака зависит от его химического состава. Из всех компонентов шлака наиболее существенно влияют на обессеривающую способность оксиды кальция и кремния. CaO ее увеличивает; SiO2 уменьшает. Поэтому обессеривающую способность шлака оценивают отношением: 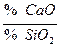 . Чем больше отношение, тем выше константа распределения
. Чем больше отношение, тем выше константа распределения 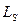 . Температура влияет на
. Температура влияет на 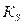 и
и 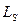 незначительно.
незначительно.
Процесс десульфурации определяется в значительной степени кинетикой взаимодействия. Чем быстрее идёт процесс, тем ближе система к состоянию равновесия и полнее используется обессеривающая способность шлака.
Большое значение имеют интенсивность перемешивания и вязкость шлака. Скорость процесса десульфурации возрастает по мере увеличения интенсивности перемешивания металла и шлака, а также понижения вязкости шлака, что может быть достигнуто повышением температуры и введением разжижающих добавок. Такой эффект связан с тем, что десульфурация расплавов железа протекает в диффузионной области и основным лимитирующим звеном процесса является переход серы из металлического расплава в шлак.
Раскисление
Раскисление - это заключительная технологическая операция плавильного процесса. Она проводится для того, чтобы снизить до минимума содержание кислорода, остающегося в расплаве после окислительного рафинирования. Кислород необходимо перевести в соединения, которые должны быть удалены из расплава.
Критерием раскислительной способности того или иного элемента является активность кислорода в металле, которая находится в равновесии с определенной концентрацией (активностью) элемента раскислителя и с продуктами раскисления, образуемыми раскислителем с кислородом.
При одновременном использовании нескольких раскислителей раскислительная способность каждого из них может увеличваться. Известно, что марганец и кремний взаимно усиливают раскислительную способность друг друга.
При выборе раскислителей необходимо отдавать предпочтение тем элементам, которые образуют оксиды, взаимодействующие между собой с образованием соединений с невысокой температурой плавления, желательно ниже температуры раскисляемого сплава, и плотностью намного меньше плотности сплава.
Требования, предъявляемые к раскислителям:
- при возможно малых концентрациях они должны обладать в условиях раскисления большим сродством к кислороду, чем раскисляемый Ме;
- остающиеся в расплаве раскислители не должны оказывать вредного влияния на свойства сплава;
- оксиды, образованные раскислителем, должны в минимальной степени растворяться в раскисляемом металле;
- нерациональные потери раскислителя должны быть минимальны;
- раскислители должны быть дешевыми и недифицитными.
Для раскисления железоуглеродистых сплавов используют C, Mn, Si, Al, Ti, Ca и др.
Процесс удаления продуктов раскисления связан не только с их природой, но и со многими побочными факторами: глубина ванны, высота ковша и др.
Эффективным средством раскисления сплавов является использование вакуума. В вакууме усиливается раскислительная способность элементов и создаются благоприятные условия для дегазации и удаления неметаллических включений. Но в вакууме возникает опасность взаимодействия жидкого металла с оксидами огнеупорных материалов футеровки.
Дата добавления: 2015-01-29; просмотров: 1128;
