Тұздар гидролизi
 Жұмыстың мақсаты
Жұмыстың мақсаты
Тұздардың гидролиздену реакцияларын зерттеу,
ортаның рН-өзгерiсін және гидролиздiң
температура мен сұйылтуға тәуелді екенін байқау.
Жұмыстың мазмұны
а) Гидролиз кезiнде қышқылдық тұздардың түзiлуi.
б) Гидролиз кезiнде негiздік тұздардың түзiлуi.
в) Бiрнеше тұздардың бірге гидролизденуi.
г) Температура мен сұйылтудың гидролизге әсерi.
Жұмыстың теориялық негізі
Гидролиз деп тұз иондары мен су иондарының арасындағы реакцияны айтады. Реакция нәтижесiнде әлсiз электролиттер түзiледі және ерітiндi ортасының рН өзгереді.
I-жағдай.
Күштi негiзден және әлсiз қышқылдан түзiлген тұздың гидролизi әлсiз қышқылдың анионы арқылы жүредi:
СО32- + НОН 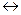 НСО-3 + ОН-
НСО-3 + ОН-
Na2CO3 + HOH 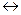 NaHCO3 + NaOH яғни pH > 7.
NaHCO3 + NaOH яғни pH > 7.
II-жағдай.
Әлсiз негiзден және күштi қышқылдан түзiлген тұздың гидролизi әлсіз негіздің катионы арқылы жүредi:
АI3+ + НОН 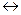 АIОН2+ + Н+
АIОН2+ + Н+
АIСI3 + НОН 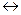 АIОНСI2 + НСI яғни pH < 7.
АIОНСI2 + НСI яғни pH < 7.
III-жағдай.
Әлсiз қышқылдан және әлсiз негiзден түзiлген тұздың гидролизi катион және анион арқылы жүреді.
NН+4 + СН3СОО- + НОН 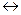 NН4ОН + СН3СООН
NН4ОН + СН3СООН
NН4СН3СОО + НОН 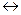 NН4ОН + СН3СООН яғни pH
NН4ОН + СН3СООН яғни pH 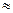 7.
7.
IV-жағдай.
Әлсiз негiзден және әлсiз қышқылдан түзiлген тұздың гидролизi бiр саты бойынша жүретін қайтымсыз процес, егер реакция нәтижесiнде түзiлген заттың бiрi газ күйiнде болса:
АI2S3 + 6HOH 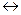 2AI(OH)3
2AI(OH)3 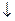 + 3H2S
+ 3H2S 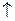 яғни pH
яғни pH 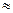 7.
7.
V-жағдай.
Бiрнеше тұздардың бірге гидролизі нәтижесiнде суда ерімейтiн немесе суда кездеспейтiн қосылыстар түзiледi.
АI2(SО4)3 + 3Nа2СО3 + 6HOH = 2АI(ОН)3 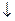 + 3Н2СО3 + 3Nа2SО4
+ 3Н2СО3 + 3Nа2SО4
2АI3+ + 3СО32- + 6НОН = 2АI(ОН)3 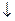 + 3Н2СО3 яғни pH
+ 3Н2СО3 яғни pH 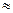 7.
7.
Дата добавления: 2014-12-08; просмотров: 2807;
