Оксид углерода
Оксид углерода (СО) образуется при неполном сгорании топлива в цилиндре двигателя в случае локального недостатка воздуха. Окисление СО в зависимости от коэффициента избытка духа протекает по-разному. При αв< 1 реакция окисления с а углерода вследствие недостатка воздуха конкурирует с реакцией окисления водорода. При этом в цепных реакциях участвует: ободный радикал ОН и атомарный водород Н, т. е.
СО + ОН→С02 + Н (7.45)
Н2+ОН→Н20 + Н (7.46)
Химическая реакция (7.46) протекает практически в условиях равновесия, а при αв< 1 идет гораздо медленнее и определяет скорость цепной реакции. При увеличении коэффициента избытка воздуха и температуры отклонение химической кинетики от равновесия мало и скорость образования СО равна
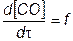 (
( 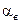 ,Т) (7.47)
,Т) (7.47)
т.е. концентрация СО снижается с увеличением αв.
При αв= 1 можно промежуточные реакции (7.45) и (7.46) заменить одной общей реакцией
СО + Н2О→С02+Н2 (7.48)
называемой реакцией водяного газа. Она имеет близкий к равновесному химическому процессу характер, что обусловлено высокими значениями избыточной концентрации атомарного водорода свободного радикала ОН, играющих основную роль в развитии цепных реакций.
При αв> 1 реакция окисления оксида углерода уже не может конкурировать с реакцией окисления водорода и протекает по следующей схеме:
СО + ОН→СО2 + Н (7.49)
О2+Н→ОН + О (7.50)
При этом во время процесса расширения более заметен неравновесный характер реакций (7.49), концентрация атомарного водорода превышает концентрацию свободного радикала ОН, поэтому реакция окисления СО замедляется.
При αв> 1,4 образование оксида углерода связано с низким значением температуры и неполным сгоранием топлива в пристеночных зонах КС. В целом реакция окисления оксида углерода (7.49) сильно зависит от температуры и в процессе расширения определяется вследствие снижения температуры. В связи с этим концентрация оксида углерода в отработавших газах двигателя практически соответствует его равновесной концентрации при температуре 1700 К.
Дата добавления: 2014-12-30; просмотров: 489;
