Основные определения.
ОСНОВНЫЕ ЗАКОНЫ ХИМИИ
Химия – одна из фундаментальных естественных наук, предметом изучения которой являются вещества, их свойства и превращения. Одной из центральных характеристик вещества является масса m. Истинные массы структурных составляющих вещества (атомов, молекул и др.) очень малы, порядка 10-24¸10-20 г, поэтому для удобства в химии принято работать не с абсолютными, а с относительными значениями масс.
Относительная атомная масса химического элемента Аr – это величина, равная отношению средней массы атомов данного элемента (с учетом процентного содержания его изотопов в природе) к 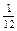 массы изотопа углерода 12 (
массы изотопа углерода 12 ( 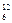 С). Значения атомных масс всех химических элементов содержатся в Периодической системе Д.И. Менделеева.
С). Значения атомных масс всех химических элементов содержатся в Периодической системе Д.И. Менделеева.
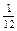 массы
массы 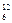 С называется атомной единицей массы (а.е.м.), т. е.
С называется атомной единицей массы (а.е.м.), т. е.
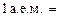
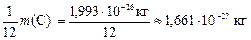 .
.
Относительная молекулярная масса вещества Mr находится как сумма Аr атомов, из которых состоит молекула.
В 1971 году в Международную систему единиц измерения (СИ) была введена единица количества вещества – моль n– такое количество вещества, которое содержит столько структурных элементарных частиц (атомов, молекул, ионов, электронов, эквивалентов и т.д.), сколько содержится атомов в 12 г изотопа углерода 12.
Число атомов в 12 г 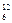 С равно 6,02×1023 атомов. Это число называется постоянной Авогадро NА, которая равна NА = (6,022045±0,000031)×1023 моль-1.
С равно 6,02×1023 атомов. Это число называется постоянной Авогадро NА, которая равна NА = (6,022045±0,000031)×1023 моль-1.
Таким образом, количество вещества можно оценить по формуле
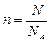 , (1)
, (1)
где N – число элементарных структурных единиц вещества.
Масса 1 моль вещества называется молярной массой M. Ее можно вычислить как отношение массы вещества m к его количеству n, кг/моль (г/моль):
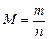 или
или 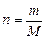 (2)
(2)
Численное значение М (в г/моль) совпадает с Mr вещества или Аr элемента.
Дата добавления: 2017-09-19; просмотров: 239;
