Различают теплоемкости при постоянном объеме и постоянном давлении, если в процессе нагревания вещества его объем или давление поддерживается постоянным.

|
|
Запишем выражение первого начала термодинамики (51.2) для 1 моль газа с учетом формул (52.1) и (53.1):
 (53.3)
(53.3)
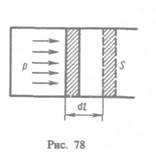
Если газ нагревается при постоянном объеме, то работа внешних сил равна нулю (см. (52.1)) и сообщаемая газу извне теплота идет только на увеличение его внутренней энергии:
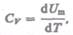 (53.4)
(53.4)
т. е. молярная теплоемкость газа при постоянном объеме 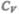 равна изменению внутренней энергии 1 моль газа при повышении его температуры на 1 К. Согласно формуле
равна изменению внутренней энергии 1 моль газа при повышении его температуры на 1 К. Согласно формуле
(50.1), 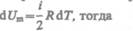
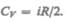 (53.5)
(53.5)
Если газ нагревается при постоянном давлении, то выражение (53.3) можно записать в виде
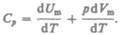
Учитывая, что 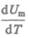 не зависит от вида процесса (внутренняя энергия идеального газа
не зависит от вида процесса (внутренняя энергия идеального газа
не зависит ни от р, ни от V, а определяется лишь температурой Т) и всегда равна  (см. (53.4)), и дифференцируя уравнение Клапейрона — Менделеева
(см. (53.4)), и дифференцируя уравнение Клапейрона — Менделеева 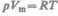 (42.4)
(42.4)
по Т (р=const), получаем
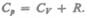 (53.6)
(53.6)
Выражение (53.6) называется уравнением Майера; оно показывает, что 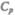 всегда больше Сv на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объема газа. Использовав (53.5), выражение (53.6) можно записать в виде
всегда больше Сv на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объема газа. Использовав (53.5), выражение (53.6) можно записать в виде
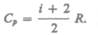 (53.7)
(53.7)
При рассмотрении термодинамических процессов важно знать характерное для каждого газа отношение 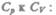
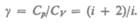 (53.8)
(53.8)
Из формул (53.5) и (53.7) следует, что молярные теплоемкости определяются лишь числом степеней свободы и не зависят от температуры. Это утверждение молекуляр-но-кинетической теории справедливо в довольно широком интервале температур лишь для одноатомных газов. Уже у двухатомных газов число степеней свободы, проявляющееся в теплоемкости, зависит от температуры. Молекула двухатомного газа обладает тремя поступательными, двумя вращательными и одной колебательной степенями свободы.
По закону равномерного распределения энергии по степеням свободы (см. § 50), для комнатных температур  Из качественной экспериментальной зависимости
Из качественной экспериментальной зависимости
молярной теплоемкости 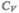 водорода (рис. 80) следует, что
водорода (рис. 80) следует, что 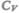 зависит от температуры: при низкой температуре (=50 К)
зависит от температуры: при низкой температуре (=50 К) 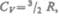 при комнатной —
при комнатной — 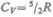 (вместо расчетных
(вместо расчетных 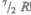 !) и при очень высокой -
!) и при очень высокой -  R. Это можно объяснить, предположив, что при низких температурах наблюдается только поступательное движение
R. Это можно объяснить, предположив, что при низких температурах наблюдается только поступательное движение
Дата добавления: 2017-04-20; просмотров: 826;
