Соединения и функции
Одной из важнейших функций крови является перенос поглощаемого в легких кислорода к органам и тканям и транспорт углекислого газа в обратном направлении.
Ключевую роль в этом процессе играют эритроциты, благодаря содержанию в них красного кровяного пигмента - гемоглобина.
Внутриэритроцитарная локализация Нb:
· Обеспечивает уменьшение вязкости крови.
· Уменьшает онкотическое давление, предотвращая потерю воды тканями.
· Предупреждает потерю Нb при фильтрации крови в почках.
По химической природе - это хромопротеид, состоящий из белка глобина (96%) и простетическая группы гема (4%). Гема содержится 4 группы. Он представляет собой протопорфирин, в центре которого расположен ион Fe++.
Содержание Fe у человека 4 - 5 г, из них в:
Нb - до 73% ;
ферментах - 16% ;
плазме крови - 0,1%.
Ключевую роль в деятельности Нb играет ион Fe++.
Функции гемоглобина:
· Транспорт О2 в виде оксигемоглобина (HHbO2). Одна молекула Нb присоединяет 4 молекулы кислорода. 1г Нb связывает 1,34мл О2
· Транспорт СО2 . В тканях карбаминовой связью присоединяет СО2 и в виде карбогемоглобина (HHbСО2) переносит его к легким.
· Участвует в поддержании кислотно-щелочного состояния (ге-моглобиновый буфер).
Соединения Нb:
1. Оксигемоглобин (НHbО2). Гемоглобин, присоединивший 4О2. В артериальной крови его содержится около 98%, а в венозной - около 60%. После отдачи О2 НHb получил название восстановленный, редуцированный гемоглобин или дезоксигемоглобин). Гемоглобин обладает высоким сродством к кислороду. Показателем сродства является Р50 - напряжение О2 в мм рт.ст., при котором 50% оксигемоглобина отдало О2 (в норме Р50 равно 27 мм рт. ст.). Снижение данного показателя свидетельствует об уменьшении сродства гемоглобина к кислороду, а увеличение его - о повышении сродства.
2.Карбогемоглобин (НHbСО2 ) - соединение гемоглобина с СО2.
3. Метгемоглобин (MetHb). Образуется под влиянием сильных оки-слителей (перманганат калия, анилин, нитриты, пирогаллол и др). При этом Fe++ превращается в Fe+++. Соединение прочное. Появляются дегенеративно измененные эритроциты, часть из них гемолизируется. При 66% насыщения крови MtHb наступает острая гипоксия.
4. Карбоксигемоглобин (НHbCО) - соединение гемоглобина с угарным газом (СО). Соединение в 150 - 200 раз прочнее НHbО2. При содержании во вдыхаемом воздухе 0,1% СО 80% Нb превращается в карбоксигемоглобин. При содержании 1% - гибель через несколько минут. В норме в крови содержится примерно 1% НHbCO. У курильщиков - до 3%, после глубокой затяжки - до 10%. При слабых отравлениях вдыхание чистого кислорода значительно ускоряет реакцию отщепления СО (в 20 раз и более).
Физиологическими соединениями Hb являются оксигемоглобин и карбогемоглобин.
5. Солянокислый гематин или гемин (образуется при взаимодействии с соляной кислотой). При высушивании образуются кристаллы специфической формы, свойственной только данному соединению. Используется в криминалистике для обнаружения пятен крови (проба Тейхмана) и в гемометрах Сали в качестве стандартного раствора (16,7г/% или 167 г/л).
Миоглобин - дыхательный пигмент или мышечный гемоглобин содержится в скелетных мышцах, миокарде. Обладает большим сродством к кислороду по сравнению с гемоглобином. Связывает до 14% О2 в организме. Его роль заключается в обеспечении кислородом мышцу в период ее сокращения, когда происходит пережатие капилляров и кровоток через ткань прекращается. В этот период главным источником кислорода является миоглобин, который затем в фазу расслабления мышц и восстановления кровотока опять “запасается” кислородом.
Синтез Нb происходит в эритробластах и нормобластах в костном мозге.
Превращения Hb в организме включают отщепление гема и образование свободного билирубина в клетках мононуклеарной фагоцитарной системы ® транспорт свободного билирубина белками крови ® превращение в печени свободного билирубина в связанную форму ® выделение его в желчный капилляр в виде желчного пигмента и с желчью в кишечник ® в виде стеркобилина, выделяется с калом. Часть билирубина выделяется с мочой (уробилин.).
При кровоизлияниях из Hb образуется белковый комплекс коллоидной формы окиси Fe - гемосидерин. Это железосодержащий пигмент ржаво-коричневого цвета.
Состояние сниженного количества Hb в единице объема крови (чаще всего при одновременном снижении количества эритроцитов) получило название анемия.
Анемия для мужчин при содержании Hb меньше 130г/л, для женщин - меньше 120г/л (при беременности - меньше 110г/л).
Причины возникновения анемий:
· Кровопотери (постгеморрагические).
· Нарушение кровообразования.
· Повышенное кроворазрушения (гемолиз).
Разновидности Hb:
· HbP - (примитивный) - на 7-12 неделе внутриутробного развития.
· HbF - фетальный (плодный) - на 9-й неделе внутриутробного развития.
· HbA - гемоглобин взрослых - появляется перед рождением.
НbF - обладает большим сродством с О2 и насыщается на 60% при таком рО2 , когда HbA матери только на 30%. Благодаря данному свойству HbF вполне обеспечивает кислородом ткани плода в условиях сравнительно низкого рО2 в артериальной крови плода. В течение 1 года жизни HbF почти полностью заменяется HbA.
Известен вид анемии - талассемия, при которой нарушен синтез HbA, но высокое содержание HbA и HbF. Эритроциты имеют вид мишени, сильно прокрашиваются по периферии и в центре. При серповидноклеточной анемии выделен гемоглобин S, отличающийся от гемоглобина А наличием в бета-цепи вместо остатка глютаминовой кислоты остатка валина.
В норме содержание Hb в крови мужчин колеблется в пределах 130 - 160г/л , в крови женщин - 115 - 145 г/л. Общее содержание Hb в крови 700 г.
Для оценки степени насыщенности эритроцитов гемоглобином вычисляют цветовой показатель (ЦП).
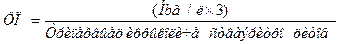
В норме ЦП = 0,8 -1,0 (нормохромные).
ЦП < 0.8 - гипохромные (при анемии).
ЦП > 1.0 - гиперхромные.
Критерием насыщения эритроцитов гемоглобином является среднее его содержание в 1 эритроците (СГЭ), рассчитанное следующим образом:



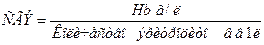

В норме СГЭ равно 27 - 31 пг.
Дата добавления: 2015-08-26; просмотров: 1863;
