Представление о химическом сродстве.
Из того факта, что одни вещества реагируют друг с другом легко и быстро, другие с трудом, третьи – совсем не реагируют, возникает предположение о наличии или отсутствии особого химического сродства между веществами.
Первое предположение о том, что мерой такого сродства является скорость реакции, пришлось оставить ввиду того, что скорость химических реакций существенно зависит от внешних причин, например, от вводимых катализаторов.
Второе предположение, по которому мерой химического сродства является тепловой эффект реакции, также пришлось оставить. Бесспорно, во многих случаях реакции идут с выделением теплоты; образование воды из водорода и кислорода, образование хлоридов из металлов и хлора, взаимодействие кислот с металлами и т.д. Однако, хорошо известны необратимые реакции, протекающие с поглощением теплоты. Кроме того, в обратимых процессах одна из реакций идет с выделением теплоты, а обратная ей реакция сопровождается поглощением теплоты. Следовательно, если мы смешаем вещества, взаимодействие которых сопровождается экзотермической реакцией, то смешение продуктов этой реакции приведет к протеканию обратной эндотермической реакции.
Вполне удачной и в настоящее время общепринятой оказалась идея Вант-Гоффа, которая затем была существенно развита бельгийским ученым Теофилом де Донде, что мерой химического сродства (А) между веществами является та максимальная полезная работа, которая совершается при обратимо протекающей между ними реакции.
В соответствии с ранее данным определением (смотри (III, 19))
W'макс. = –DG = А
Принимая во внимание (V,7), мы можем записать:
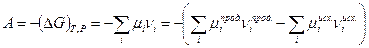
где 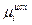 и
и  - химические потенциалы соответственно исходных реагентов и продуктов. В состоянии равновесия
- химические потенциалы соответственно исходных реагентов и продуктов. В состоянии равновесия
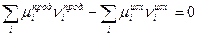 , следовательно А = 0
, следовательно А = 0
При A > 0 неравновесное состояние системы характеризуется избытком исходных реагентов и для достижения равновесия реакция должна идти слева направо; при А < 0, наоборот, система содержит избыток продуктов и реакция должна идти в противоположном направлении.
Xимическое сродство определяет собственно химический процесс, связанный лишь с изменением состава системы и не связанный с работой по преодолению сил внешнего давления.
Единица измерения химического сродства - Дж/моль.
Стандартное химическое сродство А0 определяется соотношением:
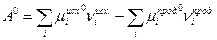
где 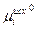 и
и  - стандартные химические потенциалы исходных реагентов и продуктов реакции соответственно. Стандартное химическое сродство связано со стандартным изменением энергии Гиббса
- стандартные химические потенциалы исходных реагентов и продуктов реакции соответственно. Стандартное химическое сродство связано со стандартным изменением энергии Гиббса 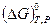 и стандартной константой равновесия реакции
и стандартной константой равновесия реакции 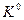 :
:
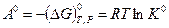
В термодинамике необратимых процессов величина  рассматривается как обобщенная термодинамическая сила, а скорость химической реакции
рассматривается как обобщенная термодинамическая сила, а скорость химической реакции 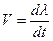 (где
(где 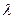 - химическая переменная и
- химическая переменная и 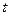 - время) - как обобщенный термодинамический поток. Произведение
- время) - как обобщенный термодинамический поток. Произведение 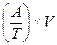 обусловливает производство энтропии в системе вследствие химической реакции.
обусловливает производство энтропии в системе вследствие химической реакции.
Дата добавления: 2015-05-21; просмотров: 960;
