История зарождения ядерной физики и создания ядерного реактора. Строение атомного ядра. Изотопы и нуклиды. Радиоактивность. Ядерные силы. Энергия связи нуклонов.
Представление об атоме, как об перво-кирпичике материи возникло в глубокой древности у философов. Древнегреческий философ Левкипп и его ученик Демокрит говорили: «Является лишь кажущимся, что вещь имеет цвет; является лишь кажущимся, что она сладкая или горькая. В действительности имеются атомы и пустое пространство. Атомы вступают во взаимную игру не по произволу и не в следствие таких сил, как любовь и ненависть, но их пути движения определяются законом природы, слепой необходимостью». И так термин атом, которым мы с вами пользуемся, придуман древними греками.
Первым исследователем, который обратился к ранним идеям греческих философов, был француз Гассенди (1592 – 1655). Он был теологом и философом и являлся современником Галилея и Кеплера, поэтому знал о первых успехах вновь возникающего тогда естествознания. В то время, после перерыва почти в 2000 лет, создались опять подходящие условия для дальнейшего развития естественно-научных познаний.
Следующий ученый физик и химик англичанин Роберт Бойль (1627 – 1691) ввел понятие химического элемента в современном смысле. Из 92 основных веществ, известных до эры получения искусственных элементов, Бойль знал лишь немногие. Тем не менее он уже совершенно ясно сформулировал задачу химии: «Необходимо установить, на какие основные вещества может быть разложена материя с помощью химических средств, и каковы эти основные вещества».
Наш соотечественник Михаил Васильевич Ломоносов является автором очень важного закона химии – «закона сохранения веса», который был высказан им в 1748 году.
В этом же направлении проводил исследования известный химик Лавуазье (1743 – 1794). Он развил идеи Михаила Васильевича и является основателем количественной химии, разрушив существовавшую в то время теорию «флагистона».
Усилиями химиков англичанина Дальтона в 1803 году, показавшего, что атомная масса является индивидуальной характеристикой атомного вещества, и нашего соотечественника Менделеева, построившего в 1869 году периодическую систему элементов, атомная теория строения вещества получила общее признание.
Следующим шагом в понимании строения атома стало открытие английским физиком Томсоном в 1897 году электрона носителя элементарного электрического заряда. Тем способом, которым был открыт электрон при изучении катодных лучей, получить частицу с положительным зарядом не удалось. Поэтому в 1904 году Томсон предлагал, что атом, представляет собой сферическое тело с равномерно распределенным положительным электричеством, в котором плавают электроны.
За год до открытия электрона французом Беккерелем было обнаружено явление радиоактивности, которое представляет собой превращение одних атомов в соседние атомы по периодической системе элементов при испускании заряженных частиц. В руках физиков оказался уникальный инструмент для исследования свойств микромира. Детектором альфа частиц стала обыкновенная фотопластинка. Исследуя прохождение коллимированного пучка альфа частиц через тонкую металлическую фольгу английский физик Резерфорд зарегистрировал альфа частицы, рассеянные на большие углы, превышающие 90 градусов. Этого эффекта модель атома Томпсона объяснить не могла. На смену этой модели Резерфорд предложил ядерную модель атома. В центре в ядре находится весь положительный заряд, а вокруг ядра вращаются электроны, несущие отрицательный заряд.
С этого момента классическая физика вступила в противоречие с физикой микромира, потому что не удавалось объяснить устойчивость атома. Разноименные заряды должны притягиваться. Быстрое вращение вокруг ядра должно приводить к излучению энергии. При помощи классической электродинамики не удавалось описать атом.
Первую стационарную модель атомного ядра с одним электроном предложил датский физик Бор в 1913 году. Бор связал устойчивость атома с квантовой природой излучения. Ядерная модель атома с электронами на устойчивых орбитах получила название планетарной моделью Резерфорда – Бора, Но она не позволяет исследовать более сложные атомные ядра. С 1920 года ядро атома водорода имеет официальный термин – протон. Однако построить атом из двух частиц протона и электрона физикам не удавалось. Однако в 1932 году открытая английским физиком Чедвиком частица нейтрон, не имеющая электрического заряда позволила построить атомное ядро.
Эту историческую справку я подготовил, опираясь на более обширный материал из книги Вернера Гейзенберга «Физика атомного ядра», составленной на основе докладов, сделанных автором в высшей технической школе в Шарлоттенбурге весной 1942 года.
Первое сообщение об открытии явления, названного делением урана, поступило из Германии в январе 1939 года. Более тщательное исследование Бором и Ферми этого явления привели к идее создания атомной бомбы. И, если Гитлер получит в руки это оружие, то человечеству грозит катастрофа. На заседании Колумбийского университета 24 февраля 1939 года Нильс Бор и Энрико Ферми сообщили, что при бомбардировке урана медленными нейтронами высвобождается огромное количество энергии.
В 1940 году армия и флот выделили Колумбийскому университету 6 тысяч долларов на построение атомного котла из графита и окиси урана. В начале 1942 года Ферми и его команду, вместе с графитово-урановым сооружением перевели в Чикаго, который стал центром исследования цепной реакции. 2 декабря 1942 года был проведен эксперимент, показавший возможность создания атомной бомбы. В этот день был зажжен первый атомный огонь на Земле в 15 часов 25 минут по Чикагскому времени. Первый атомный огонь горел 28 минут, за тем цепная реакция была прекращена. Следующий этап создания атомной бомбы выполнен был Америкой в рамках «Манхэттенского Проекта» под руководством генерала Гровса ценой в 2 миллиарда долларов. Научным руководителем проекта стал доктор Оппенгеймер. Испытание первой атомной бомбы произошло в северо-западной части базы Аламогордо. Ответственным за испытание был Отто Фриш, который вместе с Лизой Мейтнер первым понял все значение деления урана. Громадное облако, поднявшееся на высоту 12,5 километра 15 июля 1945 года вызвал взрыв, эквивалентный двадцати тысяч тон тротила. Следующие два взрыва всем хорошо известны 6 августа над городом Хиросима и 9 августа над Нагасаки. В это время в лаборатории измерительных приборов в Москве велись активные исследования под руководством Курчатова по созданию отечественного атомного оружия, а в 1946 году начал гореть ядерный огонь в реакторе Ф1, который существует по сей день.
И так, начиная с 1932 года, после открытия английским физиком Чедвиком нейтрона, все противоречия в описании атомного ядра были сняты. Любое атомное ядро характеризуется атомным номером Z и массовым числом А. Массовое число определяет количество протонов и нейтронов, а Z количество протонов. Следовательно разница А – Z определяет количество нейтронов. Например, атомный номер ядерной взрывчатки 235U равен 92. Это означает, что его ядро состоит из 92 протонов и 143 нейтронов Химическую природу элемента определяет его атомный номер, это происходит потому, что химические свойства определяются электронами, или, если быть более точными, количеством электронов на внешней оболочке атома. Поэтому химические элементы, имеющие разное число нейтронов в атомном ядре с точки зрения химии эквивалентны.
Принята следующая терминология. Атом с определенным числом протонов и нейтронов в ядре называется нуклидом. Атомы, имеющие одинаковый атомный номер, но разные массовые числа называют изотопами. То есть изотопа отличаются друг от друга количеством нейтронов в ядре. Атомы, имеющие одинаковое число нейтронов в ядре, называются изотонами. Атомы с одинаковыми мысовыми числами называются изобарами. Самый простой атом водорода имеет три изотопа: протий, дейтерий и тритий. Изотонами являются дейтерий и гелий-3. У них в составе атомного ядра по одному нейтрону. А с тритием гелий-3 является изобарами. Их массовые числа равны трем.
Большинство имеющихся в природе элементов представляют собой смесь стабильных изотопов. В природе встречаются около 280 стабильных изотопов, около 50 радиоактивных и еще более 700 радиоактивных изотопов получено искусственно с помощью различных ядерных реакций. И этот процесс получения искусственных изотопов продолжается.
Явление радиоактивности, открытое Беккерелем, состоит в том, что эти вещества испытывают спонтанное превращение, которое обычно называют радиоактивным распадом. При радиоактивном распаде атомное ядро испускает электрически заряженную частицу, либо α-частицу, которая представляет собой ядро атома гелия-4, либо β--частицу, которая представляет собой электрон, либо β+-частицу именуемую позитрон. В некоторых случаях ядро захватывает электрон с внутренней оболочки атома. Как правило, следующий элемент является радиоактивным и в свою очередь испускает заряженную частицу. Во многих случаях ядро, ядро, получившееся в результате радиоактивного распада, его обычно называют дочерним, не находится в своем основном состояние, то есть в состояние с наименьшей энергией. Такое состояние атомного ядра называют возбужденным. В течении очень короткого промежутка времени 10-15 с ядро излучает избыток энергии в виде γ-излучения. Цепочка радиоактивных превращений заканчивается стабильным изотопом. Стабильные изотопы, если построить график зависимости: по оси ординат – число нейтронов, по оси абсцисс – число протонов, то отношение числа нейтронов к числу протонов будет меняться от 1 до 1,56. Последним стабильным элементом является висмут.
Если число нейтронов и протонов в ядре какого-либо атома таково, что их отношение лежит вне области устойчивости, то ядро оказывается радиоактивным. Радиоактивные ядра спонтанно распадаются с образованием более устойчивых ядер. При этом область стабильности не является непрерывной. Например, у меди два стабильных изотопа 63Cu и 65Cu, а изотопы 62Cu и 64Cu радиоактивны.
Каждое ядро данного радиоактивного вещества имеет определенную вероятность распада в единицу времени. Эта вероятность является характерной особенностью данного вещества, причем никакими известными способами ее нельзя изменить. Величина вероятности распада не зависит от физических и химических состояний элемента при всех достигнутых температурах и давлениях. В данном веществе скорость распада в каждый момент времени прямо пропорционально имеющемуся числу рассматриваемых радиоактивных атомов. Если обозначить N число радиоактивных атомов в некоторый момент времени t, то скорость распада определяется по формуле
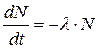
где λ – называется постоянной радиоактивного распада. Обозначим число радиоактивных ядер в начальный момент времени через N0. N – число не распавшихся ядер в момент времени t. Проинтегрировав дифференциальное уравнение в пределах от 0 до t получим
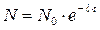
Скорость радиоактивного распада удобно выражать с помощью периода полураспада. Период полураспада определяется как время, необходимое для того, чтобы распалась половина всех имевшихся вначале радиоактивных ядер. Следовательно 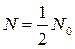
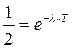
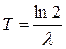
Периоды полураспада известных радиоактивных веществ меняются от долей секунды до миллиардов лет.
Возникает закономерный вопрос: «Ядро, состоящее из положительно заряженных протонов должно чем-то удерживаться в состоянии стабильности». Более того, ядро атома дейтерия, состоящего из одного протона и одного нейтрона, также является устойчивым. Следовательно, существуют силы, обеспечивающие стабильность ядра, получили название ядерных. Они превосходят по величине электростатические силы, однако, действуют на небольших расстояниях.
Ядерные силы на столько велики, что нуклоны, объединенные в ядро, уменьшаются в суммарной массе. Если бы не было изменения массы, обусловленного действием ядерных сил, то масса ядра равнялась бы сумме масс составляющих его протонов Z и нейтронов A – Z. Определение отдельных атомных масс показывает, что они в действительности всегда меньше величин, вычисленных по способу, предложенному выше. Разность между вычисленной массой и экспериментально полученной называется дефектом масс. Для определения энергии, эквивалентной дефекту массы, пользуются соотношением Энштейна между массой и энергией E=mc2.
Рисунок страница 81(Климов).
Ядерные реакции. Деление тяжелых ядер. Ядерные эффективные сечения.
Впервые, облучая, альфа частицами ядра азот, ядерную реакцию наблюдал Резерфорд в 1919 году. Эта реакция образования протона записывается 14N(α,p)17O. Ядерные реакции, в отличие от химических, при обычных условиях практически не наблюдаются. Это связано с тем, что положительно заряженные ядра взаимно отталкиваются, а ядерные силы очень короткодействующие. Это отталкивание может быть преодолено, если вещество нагреть до температуры несколько миллионов градусов или, как в опытах Резерфорда, заряженная частица должна иметь достаточную кинетическую энергию по отношению к ядру мишени. Открытый Чедвиком нейтрон, в отличие от альфа частицы, не имеет электрического заряда, поэтому может вступать в ядерные реакции при нормальной температуре. При энергии частиц до 10 МэВ ядерные реакции происходят через двустадийный механизм составного ядра. Ядро мишени поглощает бомбардирующую частицу и переходит в сильно возбужденное состояние. Это возбуждение снимается испусканием исходной или другой частицы. Возможные пути распада составного ядра называются каналами ядерной реакции. Для реакций с нейтронами рассматривают следующие каналы ядерных реакций:
Упругое рассеяние нейтрона (n,n)
Неупругое рассеяние нейтрона (n,n’)
Радиационный захват нейтрона (n,γ)
Реакция с образованием двух нейтронов (n,2n)
Реакция с образованием протона (n,p)
Реакция с образованием альфа частицы (n,α)
И, наконец, самая важная для физики ядерных реакторов, реакция деления ядер (n,f)
Деление тяжелых ядер, открытое в 1939 году Мейтнер и Фриш с одной стороны, Штрассман и Ганн – с другой. Менее чет за год появилось белее 100 публикаций, посвященных этому вопросу.
Значение реакции деления, с точки зрения использования атомной энергии основано на двух фактах. Во-первых, этот процесс сопровождается выделением сравнительно большой энергии. Один грамм разделившегося 235U дает 1 МВт·сут. тепловой энергии. Во-вторых, реакция, вызванная нейтронами, в свою очередь сопровождается вылетом нейтронов. Следовательно, при подходящих условиях процесс деления можно сделать самоподдерживающимся и энергия будет генерироваться непрерывно.
Деления ядер может быть вынужденным или спонтанных. Вероятность спонтанного деления естественных нуклидов крайне мала. Так в 1 грамме естественного урана в течении 1 часа спонтанное деление испытывает в среднем около 23 ядер. При вынужденном делении ядер, если, например, в ядро 235U попал нейтрон и образовалось промежуточное ядро 236U. В промежуточном ядре возникают колебания, приводящие к отклонению формы ядра от начальной. Возникает ситуация когда кулоновское отталкивание превосходит ядерные силы и ядро делится на две части.
В ядерной физике принято энергию элементарных частиц измерять в эВ. Один эВ это энергия, которую бы получил электрон при ускорении разностью потенциалов в 1Вольт.
1 эВ = 1,6·10-19 Дж
Понятно, что для нейтрона, не имеющего заряда, эта единица несколько условна, но обладая скоростью и массой нейтрон, следовательно, имеет кинетическую энергию, которую, используя данное соотношение, легко перевести в эВ.
Две части исходного ядра за счет работы ядерных сил превращаются в два новых ядра, которые принято называть осколками деления. Электростатическое отталкивание ускоряет осколки деления и потенциальная энергия электростатического отталкивания переходит в кинетическую энергию осколков деления. Энергию возбуждения осколки деления при переходе в основное энергетическое состояние снимают испуская нейтроны и гамма-кванты.
Нейтроны, вылетевшие из ядра в результате процесса деления, могут быть разделены на две группы: мгновенные нейтроны и запаздывающие нейтроны. Мгновенные нейтроны, составляющие более 99% общего числа нейтронов, полученных при делении, вылетают в чрезвычайно короткий промежуток времени – порядка 10-14 секунды после деления. Энергия мгновенных нейтронов лежит в широком интервале, однако большинство мгновенных нейтронов имеют энергию 1 – 2 МэВ.
После торможения в среде осколки деления превращаются в нейтральные атомы в основных энергетических состояниях и называются продуктами деления. Первичные атомы-продукты, испытав в среднем по три радиоактивных распада, становятся стабильными ядрами. В редких случаях таких превращений испускаются запаздывающие нейтроны.
Таблица стр. 155. (В кн. А.Н. Климова)
При делении 235U тепловыми нейтронами образуется около сорока различных пар осколков, преимущественно неравной массы. Наибольший выход относится к массовым числам 95 и 139 и составляет 6 %. Самое легкое и самое тяжелое ядра, зарегистрированные при делении, имеют массовые числа 72 и 161 соответственно.
График стр. 158. (В кн. А.Н. Климова)
Для всех приведенных ядерных реакций с нейтронами вероятность их протекания в огромной степени зависит от энергии нейтрона, попадающего в ядро мишени. Количественно эту вероятность можно выразить, введя понятие микроскопического сечения. Для объяснения физического смысла сечения предположим, что однородный пучок нейтронов падает перпендикулярно на слой вещества толщиной в один атом и вызывает в нем за данное время определенное число С некоторых ядерных реакций, например реакций захвата, приходящихся на 1 см2, и пусть I есть число нейтронов, упавших за это же время на 1 см2 мишени. Тогда ядерное микроскопическое сечение σ данной реакции определяется как среднее число процессов, происходящих на один падающий нейтрон в пучке и на одно ядро вещества-мишени, то есть
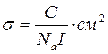
Так как величины микроскопических сечений очень малы, их выражают в очень мелких единицах площади, получивших название барны.
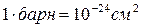
Если просуммировать вероятности процесса для всех ядер рассматриваемого материала мы получим макроскопическое сечение вещества для данного процесса.
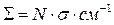
Где N число ядер данного вещества в 1 см3.
Количественное описание нейтронных взаимодействий возможны только при известных сечениях. В отсутствии последовательной теории ядерных сил нейтронные сечения не могут быть вычислены и должны определяться на опыте.
Следует ввести понятие полного сечения взаимодействия нейтронов. Если для данной энергии нейтронов просуммировать все возможные способы взаимодействия нейтронов с данным веществом, то эту величину называют полным сечением взаимодействия.
Исследуя различными способами сечения ядерных реакций, было получено, что в зависимости от энергий нейтронов, оно ведет себя следующим образом:
для энергий около 1 эВ и ниже, сечение ядерных реакций подчиняется закону 1/V
для диапазона энергий 1 – 100 эВ начинается область резонансов. Нейтронные сечения имеют сложную «пикообразную» структуру.
для энергий от 100 эВ до 10 кэВ начинается область неразрешенных резонансов
от 10 кэВ и выше сечения ядерных реакций может приобрести пороговый характер.
Кроме того, для некоторых ядерных реакций для заданных энергетических интервалов сечение этой реакции может равняться нулю.
Сечение рассеяния нейтронов
Подразделяется на потенциальное, когда не образуется составное ядро, и резонансное, в случае образования составного ядра. Это наиболее вероятный процесс взаимодействия нейтрона с ядром. В этом случае взаимодействие нейтрона с ядром рассматривается как упругое.
Неупругое сечение рассеяния нейтронов
Происходит, как правило, для нейтронов высоких энергий. При этом, энергия нейтрона, испускаемого промежуточным ядром, значительно уменьшается и, кроме нейтрона, испускаются гамма-кванты.
Радиационный захват нейтрона
Происходит в области тепловых и промежуточных нейтронов. Для быстрых нейтронов радиационный захват нейтронов маловероятен.
Реакции с образованием заряженных частиц.
Происходят для быстрых нейтронов, и, как правило, являются пороговыми.
Реакция с образованием двух нейтронов
Так же является пороговой и происходит для быстрых нейтронов.
Реакция деления ядер
Для нуклидов 233U, 235U и 239Pu, называемых делящимися, реакция происходит для нейтронов всех энергий, но сечение реакции для медленных нейтронов заметно выше, чем для быстрых нейтронов. Для нуклидов 238U, 232Th, 237Np и другие, называемых делимыми, сечение деления имеет пороговый вид, и составляет величину в несколько барн.
| <== предыдущая лекция | | | следующая лекция ==> |
| Классификация измерений | | | Общая характеристика психологической безопасности образовательной среды |
Дата добавления: 2017-12-05; просмотров: 957;
