Общие особенности гетерогенных процессов
При переходе от формально-кинетических (микрокинетика) закономерностей протекания химических реакций к осуществлению химико-технологических процессов в условиях реального производства (макрокинетика) возникает необходимость учета факторов движения реакционных потоков (гидродинамического режима) в технологических аппаратах, особенно в реакционных аппаратах - реакторах.
Для гомогенных реакций, в том числе для реакций в жидкой фазе, диффузия при переносе вещества из одной точки реакционного пространства в другую, в частности в реакторах больших размеров, оказывает влияние на кинетические показатели процесса. Однако обычно диффузионные процессы протекают с достаточно большой скоростью, особенно при интенсивном перемешивании, и существенно не влияют на скорость химического взаимодействия (макрокинетические закономерности мало отличаются от микрокинетических).
Для гетерогенных процессов учет скорости переноса вещества, особенно от фазы к фазе, значительно более важен вследствие сложности этой стадии. Поэтому зачастую скорость гетерогенного процесса определяется не скоростью химической реакции, а скоростью процессов переноса. Следует также отметить, что для большинства химических реакций, используемых в химико-технологических процессах, характерно протекание с участием веществ, находящихся в разных фазах. Поэтому необходимо детальное рассмотрение процессов, протекающих в многофазных системах. В зависимости от того, в каких фазах находятся участники реакции, выделяют различные двух- и трехфазные системы. Несмотря специфические различия, все они объединены одним общим признаком: прежде чем произойдет химическая реакция, должен осуществиться перенос реагентов из ядра потока одной фазы к поверхности раздела фаз или в объем другой фазы.
Гетерогенные процессы протекают, как правило, на поверхности раздела фаз или на поверхности твердого катализатора в газофазных процессах.
Характерной чертой любого гетерогенного процесса является многостадийность - обязательное наличие наряду с одной или несколькими чисто химическими стадиями (химическими реакциями) стадий, которые можно охарактеризовать как физические (так как при их протекании не происходит химических превращений). Последние связаны с переносом вещества от одной фазы к другой, причем концентрации вещества в разных фазах (или же в ядре фазы и на поверхности раздела) различны. Разность концентраций является движущей силой этих процессов переноса (диффузии).
При протекании гетерогенных процессов собственно химическая стадия может представлять собой как гетерогенную, так и гомогенную химическую реакцию. Например, гетерогенным будет взаимодействие кислорода с сульфидами металлов при обжиге различных сульфидных руд. Однако реакция окисления молекулярным кислородом жидких углеводородов протекает как гомогенная, хотя реагенты и находятся в разных фазах, так как в химическую реакцию вступает не газообразный, а растворенный кислород. Гетерогенной в этом случае будет не химическая реакция, а предшествующая ей диффузионная стадия растворения кислорода.
Таким образом, гетерогенные процессы многостадийны. В общем случае скорости отдельных стадий, составляющих гетерогенный процесс, могут существенно различаться и в разной степени зависеть от изменения параметров технологического режима. Например, такой фактор, как температура, с разной интенсивностью влияет на скорость химической реакции и скорость переноса веществ путем диффузии. При рассмотрении скорости гетерогенного процесса с использованием уравнения 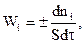 будем учитывать, что скорость не зависит от площади поверхности раздела фаз.
будем учитывать, что скорость не зависит от площади поверхности раздела фаз.
Так как конечный результат любого химико-технологического процесса - образование продукта в результате химического превращения, то скорость гетерогенного процесса в любом случае не может быть выше скорости химической реакции. Как бы быстро ни осуществлялся перенос вещества от одной фазы к другой, сам по себе этот перенос еще не приводит к образованию продукта. Одновременно скорость гетерогенного процесса не может быть больше и скорости диффузионного переноса вещества, так как он предшествует химической реакции.
При рассмотрении гетерогенных процессов выделяют две крайние, принципиально различающиеся ситуации:
- Скорость химической реакции при данном режиме осуществления процесса мала по сравнению со скоростью диффузии на стадиях, предшествующих реакции. Интенсификация гетерогенного процесса в целом может быть достигнута при таком изменении технологического режима, которое приведет к интенсификации химической стадии. Такие гетерогенные процессы принято называть процессами, протекающими в кинетической области.
- Скорость химической реакции велика и превышает скорость диффузии. Тогда для увеличения производительности и интенсификации процесса нужно стремиться к устранению тормозящего влияния диффузии. Этот случай соответствует диффузионной области протекания гетерогенного процесса.
Дата добавления: 2017-11-04; просмотров: 2506;
