Политропный процесс.
Политропным процессом называется процесс, все состояния которого удовлетворяются условию:
P· nn = Const, (4.24)
где n – показатель политропы, постоянная для данного процесса.
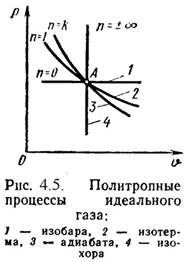
Изобарный, изохорный, изотермический и адиабатный процессы являются частными случаями политропного процесса (Рис.4.5):
при n = ± ¥ n = Const, (изохорный),
n = 0 P = Const, (изобарный),
n = 1 T = Const, (изотермический),
n = l P· n = Const, (адиабатный).
 Работа политропного процесса определяется аналогично как при адиабатном процессе:
Работа политропного процесса определяется аналогично как при адиабатном процессе:
l = R·(T1 – T2) / (n – 1); (4.25)
l = R·T1·[1 – (n 1/ n 2) n-1] /(n – 1); (4.26)
l = R·T2·[1 – (P2/P1) (n-1)/ n] /(n – 1). (4.27)
Теплота процесса:
q = cn ·(T2 – T1), (4.28)
где cn = cv ·(n - l)/(n – 1) – массовая теплоемкость (4.29)
политропного процесса.
Тема 5. Термодинамика потока.
5.1. Первый закон термодинамики для потока.
5.2. Критическое давление и скорость. Сопло Лаваля.
5.3.Дросселирование.
Первый закон термодинамики для потока.
На практике при рассмотрении рабочих процессов машин, аппаратов и устройств, встречаются задачи изучении закономерностей движения рабочих тел (газов, пара и жидкостей).
Уравнение 1-го закона термодинамики для потока газа при следующих допущениях:
· движение газа по каналу установившееся и неразрывное;
· скорости по сечению, перпендикулярному оси канала, постоянны;
· пренебрегается трение частичек газа друг другу и о стенки канала;
· изменение параметров по сечению канала мало по сравнению их абсолютными значениями,
имеет вид:
q = Du + De + lпрот. + lтехн. , (5.1)
где De = (w22 – w21)/2 + g·(z2 –z1) – изменение энергии системы,
состоящий из изменения кинетической и потенциальной энергий;
w1 ,w2 – скорости потока в начале и в конце канала;
z1 , z2 – высота положения начала и конца канала.
1. lпрот. = P2·n 2 – P1·n 1– работа проталкивания, затрачиваемая на движения потока;
2. lтехн. – техническая (полезная) работа (турбины, компрессора, насоса, вентилятора и т.д.).
3.
q = (u2 – u1) + (w22 – w21)/2 + g·(z2 –z1) + P2·n 2 – P1·n 1 + lтехн. (5.2)
Введем понятия энтальпии, который обозначим через величину:
h = u + Pх , (5.3)
h2 = u2 + P2·n 2 ; h1 = u1 + P1·n 1 . (5.4)
Тогда уравнение 1-го закона термодинамики для потока газа будет иметь вид:
q = h2 – h1 + (w22 – w21)/2 + g·(z2 –z1) + lтехн. (5.5)
Дата добавления: 2017-11-04; просмотров: 131;
