ХАРАКТЕРИСТИКА И СВОЙСТВА РАСТВОРОВ.
Раствор– термодинамическая устойчивая гомогенная система переменного состава, образованная из двух и более компонентов.
Раствор – менее упорядоченная система, чем растворитель и растворенное вещество по отдельности. По этой причине растворение сопровождается значительным увеличением энтропии. В соответствии с формулой 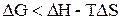 , когда ΔS>0, энергия Гиббса ΔG<0, т.е. процесс растворения становиться самопроизвольным.
, когда ΔS>0, энергия Гиббса ΔG<0, т.е. процесс растворения становиться самопроизвольным.
Кроме того, в большинстве случаев процесс растворения сопровождается выделением теплоты (ΔН<0), что также способствует более интенсивному протеканию самопроизвольного процесса. Достаточно вспомнить самопроизвольный процесс растворения серной кислоты в воде, который сопровождается бурным выделением теплоты. Реже наблюдается поглощение теплоты, например, при растворении нитрата аммония NH4NO3 в воде. Но и в этих условиях энтропийный фактор превышает энтальпийный, и согласно условию 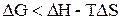 , ΔG<0, т.е. процесс растворения будет также самопроизвольным.
, ΔG<0, т.е. процесс растворения будет также самопроизвольным.
В связи с самопроизвольностью процесса растворения в природе чистые вещества, состоящие из одного компонента, почти не встречаются.
Таким образом, процесс образования растворов происходит самопроизвольно и обусловлен уменьшением энергии Гиббса, dG<0. Если химический потенциал растворяемого компонента (твердого, жидкого или газообразного) обозначить через µik, а в растворе через µip, то изменение энергии Гиббса при растворении ni числа молей вещества равно:
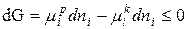 (1)
(1)
(Знак меньше соответствует самопроизвольному процессу, а знак равенства – равновесному).
Растворение возможно, когда выполняется условие
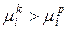 (2)
(2)
После образования раствора и достижения равновесного состояния, когда dG=0, следует
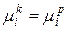 (3)
(3)
Условия, выражаемые соотношениями 1,2,3, справедливы для всех растворов, независимо от агрегатного состояния его компонентов.
Дата добавления: 2017-09-19; просмотров: 295;
