Эквивалент. Молярная масса эквивалента.
При количественных расчетах не обязательно записывать уравнение химической реакции и подбирать коэффициенты, если использовать понятие эквивалент и закон эквивалентов.
Эквивалентом Э(Х)называют некую реальную или условную частицу (атом, молекулу, ион, радикал и т.п.), которая может присоединять, замещать или быть каким-либо другим образом равноценна 1 моль атомов водорода или ионов Н+ в химических реакциях. В общем случае эквивалент элемента или вещества Х можно найти по формуле
Э(Х) = 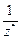 ,
,
где z* - число эквивалентности, равное тому количеству атомов или ионов водорода, которое эквивалентно (равноценно) частице Х.
Масса 1 моль эквивалента вещества или элемента Х называется молярной массой эквивалента МЭ(Х)(г/моль). Ее можно рассчитать по формуле:
МЭ(Х) = М(Х) × Э(Х) = 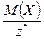 .
.
Число эквивалентности z* для химического элемента, входящего в состав какого-либо вещества, равно модулю степени окисления (С.О.), проявляемой данным элементом в химическом соединении. Таким образом, расчет молярной массы эквивалента элемента следует вести по формуле
МЭ(Элемент) = 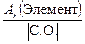 . (9)
. (9)
Для простого одноатомного вещества (например: Mg, P, S и т.д.) z* равно наиболее характерной валентности В элемента простого вещества. Тогда:
МЭ(Х) = 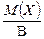 . (10)
. (10)
Правила определения значения z* веществ и формулы для расчета их молярных эквивалентных масс во всех других случаях приведены в табл.1.
При решении задач с участием газообразных веществ обычно пользуются не МЭ, а молярным эквивалентным объемом вещества VЭ, то есть объемом, который занимает 1 моль эквивалентов газа. Расчет VЭ газа (в дм3/моль) при н.у. следует вести по формуле
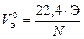 , (11)
, (11)
где Э – эквивалент элемента, составляющего газ; N – число атомов элемента в молекуле газа; 22,4 – молярный объем газа при н.у., дм3/моль.
Достаточно часто уравнения химических реакций записывают в сокращенно-ионной форме. Для ионов МЭ вычисляют по формуле
МЭ(иона) = 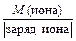 . (12)
. (12)
Таблица 1
Дата добавления: 2017-09-19; просмотров: 623;
