Внутрішня енергія ідеального одноатомного газу пропорційна температурі і не залежить від об’єму та інших макропараметрів.
Зміна внутрішньої енергії маси ідеального газу відбувається тільки у разі зміни його температури T.
Якщо газ не одноатомний, то його молекули рухаються не тільки поступально, а й обертаються. Внутрішня енергія таких газів дорівнює сумі енергій поступального і обертального рухів.
У реальних газах, рідинах і твердих тілах середня потенціальна енергія взаємодії молекул не дорівнює нулю, тому їх внутрішня енергія залежить від об’єму речовини поряд з температурою.
Внутрішню енергію термодинамічної системи можна змінити двома способами:
1) виконанням роботи;
2) теплопередачею.
Теплопередачею або теплообміном називають процес передачі енергії від одного тіла до іншого без виконання роботи. Теплопередача може відбуватися такими способами:
1) теплопровідність;
2) випромінювання;
3) конвекція (перемішування).
Кількісну міру зміни внутрішньої енергії тіла під час теплообміну називають кількістю теплоти Q. Якщо теплота передана тілу в результаті нагрівання чи охолодження, то експериментально встановлено, що
Q = cm(T2 – T1),
де c – коефіцієнт пропорційності, скалярна фізична величина, що називається питомою теплоємністю і яка чисельно дорівнює кількості теплоти, що відбирається або надається 1 кг речовини у разі зміни її температури на 1К.
Одиниця кількості теплоти в СІ – джоуль: [Q] = Дж. Позасистемна одиниця кількості теплоти – калорія (кал). Калорію визначають як кількість теплоти, яку необхідно передати одному граму води, щоб збільшити його температуру на один градус Цельсія. 1 кал = 4,18 Дж.
Питому теплоту в СІ вимірюють в джоулях на кілограм на кельвін: 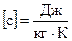 .
.
Для води 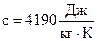 . Це досить велике значення питомої теплоємності, тому змінити температуру певної маси води досить важко. З цієї причини воду використовують як теплоносій у системах опалення. Велика теплоємність води зумовлює зменшення різких перепадів температури біля поверхні Землі, яка на 2/3 покрита водою.
. Це досить велике значення питомої теплоємності, тому змінити температуру певної маси води досить важко. З цієї причини воду використовують як теплоносій у системах опалення. Велика теплоємність води зумовлює зменшення різких перепадів температури біля поверхні Землі, яка на 2/3 покрита водою.
2. Спираючись на досліди, проведені в середині ХІХ ст., англійський фізик Джоуль та німецький Майєр, і найповніше Гельмгольц, установили закономірність, згідно з якою кількість енергії в природі незмінна, вона лише переходить від одних тіл до інших або перетворюється з одного виду в інший. Це твердження називають законом збереження і перетворення енергії. Цей закон універсальний та застосовний до всіх явищ природи.
Закон збереження енергії, поширений на теплові явища, називають першим законом термодинаміки.
У термодинаміці розглядаються тіла, положення центра тяжіння яких майже не змінюється. Механічна енергія таких тіл залишається незмінною. Змінюватися може лише внутрішня енергія U. Зміна U тіла може відбуватися за рахунок виконання роботи А або теплопередачі. У загальному випадку у разі переходу системи з одного стану в інший U змінюється одночасно як за рахунок виконання роботи, так і за рахунок теплопередачі. Саме для таких загальних випадків і застосовують перший закон термодинаміки: зміна U системи під час її переходу з одного стану в інший дорівнює сумі роботи зовнішніх сил A’ і кількості теплоти, що передається системі Q:
DU = A’ + Q.
Внутрішня енергія змінюється внаслідок виконання роботи і шляхом теплообміну. В кожному стані система має певну внутрішню енергію U. Робота і кількість теплоти не містяться в тілі, а характеризують зміни його U.
За допомогою першого закону термодинаміки можна робити важливі висновки про характер процесів, що відбуваються. Розрізняють різні процеси, під час перебігу яких одна з фізичних величин залишається незмінною (ізопроцеси).
Ізотермічний процес. Якщо T = const внутрішня енергія системи не змінюється. Уся передана газу кількість теплоти витрачається на виконання роботи над зовнішніми тілами: Q = A
Ізобарний процес. Кількість теплоти Q, передана газу за сталого тиску, витрачається на зміну його внутрішньої енергії і на виконання ним роботи над зовнішніми тілами: Q = DU + A
Адіабатний процес – процес, що відбувається в теплоізольованій системі (немає обміну енергією із зовнішніми тілами). При цьому Q = 0 і змінити внутрішню енергію системи можна лише за рахунок виконання над нею роботи: DU = A
Закон збереження і перетворення енергії стверджує, що кількість енергії за будь-яких її перетворень незмінна, але нічого в ньому не вказує на те, які енергетичні перетворення можливі. Однак багато процесів, цілком допустимих з точки зору закону збереження енергії, ніколи не відбуваються в дійсності. Наприклад, нагріте тіло, поступово охолоджуючись, передає свою енергію більш холодним тілам, які його оточують. Зворотний процес передачі теплоти від холодного тіла до гарячого самовільно відбуватися не може. Кількість таких прикладів можна навести безліч. Усі вони свідчать, що процеси в природі мають певну спрямованість. У зворотному напрямі вони самовільно відбуватися не можуть.
3.Запаси внутрішньої енергії в земній корі й океанах можна вважати практично необмеженими. Але володіти запасами енергії ще недостатньо, необхідно вміти за рахунок енергії приводити в рух верстати, засоби транспорту, машини, обертати ротори генераторів електричного струму тощо. Людству потрібні двигуни, тобто пристрої, здатні виконувати роботу. Більша частина двигунів на землі – теплові двигуни, тобто пристрої, які перетворюють внутрішню енергію палива в механічну енергію. Для того, щоб двигун виконував роботу, необхідна різниця тисків по два боки поршня двигуна або лопастей турбіни. Незважаючи на велику різноманітність видів теплових двигунів, усі вони мають загальний принцип дії.
У роботі двигунів можна виділити такі загальні ознаки:
1) у будь-якому тепловому двигуні відбувається перетворення енергії палива в механічну енергію;
2) для роботи теплового двигуна потрібні нагрівник, холодильник і робоче тіло. У процесі роботи теплового двигуна робоче тіло забирає від нагрівника певну кількість теплоти Q1 і перетворює частину цієї теплоти в механічну енергію, а неперетворену частину теплоти Q2 передає холодильнику. За законом перетворення і збереження енергії Q1 = Q2 + A;
3) робота будь-якого теплового двигуна полягає у повторюванні циклів зміни стану робочого тіла.
Широке застосування теплових двигунів для добування зручної у використанні енергії найбільше впливає на навколишнє середовище порівняно з усіма іншими видами виробничих процесів. За законами термодинаміки електричну й механічну енергію неможливо виробляти без відведення в навколишнє середовище значних кількостей теплоти. Це може призвести до підвищення середньої температури на Землі і створити загрозу підвищення рівня Світового океану.
Під час спалювання палива атмосфера забруднюється попелом, азотистими та сірчаними сполуками, шкідливими для здоров’я людей. Особливо суттєве це забруднення у великих містах і промислових центрах. Більше половини всіх забруднень атмосфери створює транспорт. Крім оксиду вуглецю, викидаються в атмосферу 2-3 млн. т свинцю. Сполуки свинцю додають в автомобільний бензин для запобігання детонації палива в двигуні, тобто дуже швидкого згоряння палива. З метою зменшення таких викидів дедалі більше випускається автомобілів, у яких замість бензинових використовують дизельні двигуни, у паливо яких не додають сполук свинцю. Однак найбільш перспективними вважаються електромобілі і автомобілі, які працюють на водні. Продуктом згоряння у водневому двигуні є звичайна вода.
Застосування теплових двигунів призводить до значного споживання кисню, який виробляється зеленими рослинами (10-25%), через що його кількість в повітрі постійно зменшується.
Застосування парових турбін на електростанціях потребує відведення великих площ під ставки, в яких охолоджується відпрацьована пара. Зі збільшенням потужностей електростанцій різко зростає потреба у воді. Для економії площ і водних ресурсів споруджуються комплекси електростанцій, насамперед атомних, із замкненим циклом водопостачання.
Одним із заходів захисту довкілля є встановлення різного роду фільтрів як на теплових станціях, так і на автомобільних двигунах. Розробляються зразки газотурбінних, роторних і навіть парових двигунів.
Дата добавления: 2016-10-17; просмотров: 1515;
