Щелочный гидролиз галогенидов
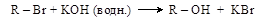
6. Восстановление сложных эфиров. Специальными восстановителями (литийалюминийгидрид LiAlH4) могут быть синтезированы высокомолекулярные спирты из сложных эфиров
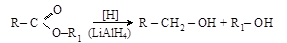
7. В промышленности широко используется получение этилового спирта брожением крахмалосодержащего сырья (спирт-ректи-фикат) или гидролизом целлюлозы (спирт-гидролизат). Последний содержит большое количество метанола в качестве примеси. Для предотвращения применения гидролизата в пищевых целях его денатурируют (добавляют вещества, придающие цвет и резко неприятный запах) – получают спирт-денатурат.
При ацетонобутиловом брожении углеводов получают (вместе с ацетоном) бутанол-1, применяемый в качестве растворителя лаков и красок, для синтеза масляной кислоты и сложных эфиров.
8.1.5. Использование спиртов
В наибольших объемах в пищевой промышленности используется этанол (спирт-ректификат) – для изготовления различных спиртных напитков.
Бензиловый спирт (C6H5–CH2OH) – компонент ароматообразующих веществ пшеничного хлеба. Изоамиловый спирт (3-метилбутанол-1) является исходным для получения уксусноизоамилового эфира («грушевая эссенция)», используемого в приготовлении конфет, фрукто-
вых вод.
Все спирты как высоко реакционноспособные вещества являются исходными для получения самых разнообразных химических продуктов: альдегидов, кетонов и карбоновых кислот; галогенопроизводных и непредельных углеводородов; каучуков и пластмасс и др. Являются хорошими растворителями многих органических веществ. Широко используются в парфюмерной промышленности. Так, 2-фенил-этанол (C6H5–CH2–CH2–OH) является главной составной частью «розового масла» – стабилизатора запахов, непременного компонента духов.
8.2. МНОГОАТОМНЫЕ СПИРТЫ (полиолы)
Многоатомными называются спирты, содержащие в молекуле больше одной оксигруппы. С одним атомом углерода может быть связана не более чем одна оксигруппа. Геминальные полиолы неустойчивы.В момент образования они, за редким исключением*, отщепляют воду, превращаясь в альдегиды (а), кетоны (б) или карбоновые кислоты (в)
|
|
|
|
|
|
|
|
|
|
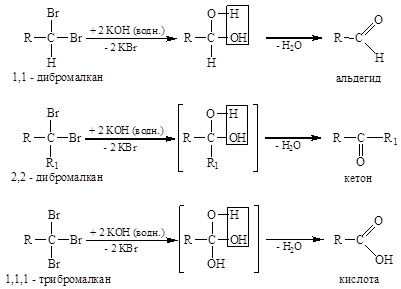
8.2.1. Изомерия и номенклатура
Изомерия многоатомных спиртов обусловлена изменениями структуры С-скелета и различным положением оксигрупп.
Некоторые полиолы имеют тривиальные названия (этиленгликоль, глицерин, инозит и др.). Двухатомные спирты называются гликолями. Гликоли с оксигруппами у соседних углеродов называют a-гликолями;
в b-гликолях эти углероды разделены одной метиленовой группой,
––––––––––––––––––––––––––
|
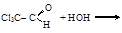
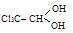 (кристаллич. вещество)
(кристаллич. вещество)
хлораль хлоральгидрат (Т пл. = 51,7°)
в g-гликолях – двумя метиленовыми группами:
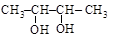
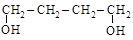
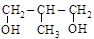
бутандиол-2,3 бутандиол-1,4 2-метилпропандиол-1,3
(a-гликоль) (g-гликоль) (b-гликоль)
Диолы различных структур являются основой диольных липидов.
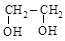
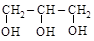
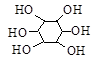
этиленгликоль глицерин инозит
этандиол-1,2 пропантриол-1,2,3 гексаоксициклогексан
8.2.2. Свойства полиолов
Важнейшими из многоатомных спиртов являются этиленгликоль и глицерин. Это вязкие, сладкие на вкус жидкости, тяжелее воды, хорошо растворимые в воде, в низших спиртах, в ацетоне, но не растворимые в жирах, бензоле, бензине. Кипят при гораздо более высоких температурах, чем одноатомные спирты с соответствующим числом атомов углерода, за счет дополнительных водородных связей (табл. 12).
Высшие полиолы (тетриты, пентиты, гекситы и др.) – бесцветные кристаллы сладкого вкуса, хорошо растворимые в воде.
По химическим свойствам гликоли и глицерины похожи на одноатомные спирты. Отличия: повышенная подвижность атомов водорода оксигрупп и возможность участия в реакциях как одной, так и нескольких оксигрупп.
1. Алкоголяты образуются при взаимодействии не только со щелочными металлами, но и со щелочами и даже с гидроксидами тяжелых металлов
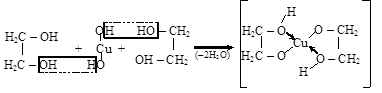 гликолят меди
гликолят меди
(внутрикомплексное соединение)
Реакция растворения осадка гидроксида меди (II) сопровождается ярким внешним эффектом (образуется синий раствор) и является качественной на многоатомные спирты.
2. Сложные эфиры легко образуются и с органическими, и с неорганическими кислотами
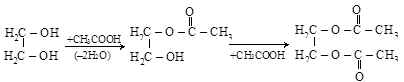
этиленгликоль неполный эфир полный эфир
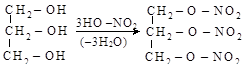
глицерин тринитроглицерин
3. Окисление протекает легко. Могут образовываться различные продукты
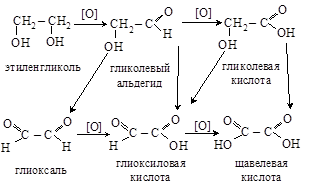
4. Дегидратация протекает по-разному в зависимости от условий реакции и строения исходного спирта:
(а) из a-гликолей получаются эпоксиды
|
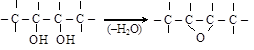
(б) из b-гликолей – непредельные спирты
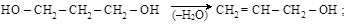
пропандиол-1,3 аллиловый спирт
(в) g-гликоли образуют циклические эфиры
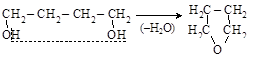
бутандиол-1,4 тетрагидрофуран
8.2.3. Получение и применение полиолов
Получают многоатомные спирты теми же способами, что и одноатомные, только вводится несколько гидроксилов
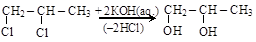
1,2-дихлорпропан пропандиол-1,2
Есть и специфические способы:
(а) реакция Вагнера (мягкое окисление алкенов)
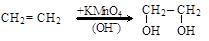
этилен этиленгликоль
(б) гидролиз a-оксидов (эпоксидов)
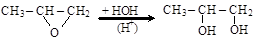
окись пропилена пропандиол -1,2
(в) глицерин в промышленности получают гидролизом (омылением) жиров
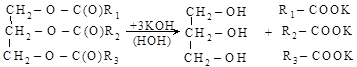
жир глицерин мыла
Многоатомные спирты – важные продукты химической промышленности, широко применяются как сами, так и их различные производные.
Этиленгликоль используется для приготовления антифризов (его водные растворы замерзают при очень низких температурах) и является промпродуктом получения пластмасс и искусственных волокон; используется в текстильной, парфюмерной, табачной и др. отраслях промышленности.
Диоксан – простой циклический эфир этиленгликоля – хороший органический растворитель
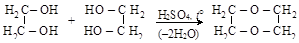
этиленгликоль диоксан
Глицерин широко используется в пищевой промышленности (для приготовления ликеров и безалкогольных напитков), в бумажной и кожевенной (для предохранения материала от высыхания), в парфюмерии (входит в состав различных кремов и мазей).
Важнейшие производные глицерина – нитроглицерины (взрывчатка и сердечное лекарство) и глифталевые смолы – полиэфиры глицерина и фталевой кислоты, применяемые для изготовления лаков.
8.3. Фенолы и нафтолы
Фенолы – оксипроизводные бензола и его гомологов, в молекулах которых гидроксил непосредственно связан с бензольным ядром. Нафтолы – оксипроизводные нафталина.
Как и спирты, фенолы бывают одно- и многоатомными. Важнейшие их представители:
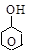
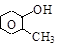
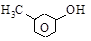
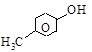
фенол о-крезол м-крезол п-крезол
(оксибензол) 2-, 3- и 4-окситолуолы (или метилфенолы)
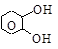
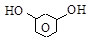
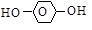
пирокатехин резорцин гидрохинон
(о-диоксибензол) (м-диоксибензол) (п-диоксибензол)
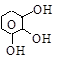
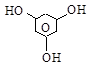
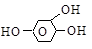
пирогаллол флороглюцин оксигидрохинон
[1,2,3- [1,3,5- [1,2,4-триоксибензолы]
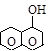
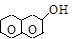
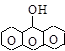
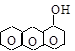
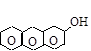
a-нафтол b-нафтол g-антрол a-антрол b-антрол
8.3.1. Физические свойства
Фенолы – кристаллические вещества или высококипящие жидкости, обладающие сильным характерным запахом. Ядовиты. Плотность фенолов около 1 г/см3. По сравнению с соответствующими циклическими спиртами, фенолы имеют более высокие температуры кипения и лучше растворяются в воде. С увеличением числа гидроксилов растворимость фенолов улучшается.
Т а б л и ц а 13
Дата добавления: 2016-04-14; просмотров: 2149;
