Постулати Бора. Походження лінійчатих спектрів
В теорії Бора розглядається будова та процеси випромінювання атома водню та воднеподібних атомів, тобто іонів, які складаються з ядра та одного електрона (He+, Li2+, Be3+, …). Заряд ядра дорівнює +Ze, де Z –атомний номер елемента, e – елементарний заряд. В простішому варіанті теорії Бора вважається, що електрон рухається в полі ядра по круговій орбіті під дією кулонівської сили, яка і надає електрону доцентрового прискорення. Справедливість такого припущення витікає з результатів дослідів Резерфорда, які свідчать, що закон Кулона виконується принаймні до відстаней між зарядами ~ 10–14 м, що на чотири порядки менше розміру атомів. Згідно законам класичної механіки, електрон може обертатися навколо ядра по круговій орбіті будь-якого радіуса, тобто ніяких обмежень на орбітальний рух електрона не існує, отже, і повна механічна енергія електрона в атомі може набувати довільних значень. Але Бор, всупереч таким висновкам класичної механіки, формулює постулати про існування певних обмежень на рух електрона в атомі, стверджуючи, по суті, існування деяких додаткових (не класичних) законів руху та випромінювання в атомних системах.
Перший постулат(про існування стаціонарних станів). Електрон в атомі може здійснювати стійкий рух лише по певних, дозволених орбітах, які називаються стаціонарними. Обертаючись по будь-якій з стаціонарних орбіт, електрон не випромінює електромагнітні хвилі, а отже повна енергія електрона (енергія атома) в стаціонарних станах не змінюється. Кожному стаціонарному стану атома відповідаєстрого визначена енергія, тобто енергія атома може дорівнювати лише одному із значень дискретного ряду E1, E2, … En, … (E1 < E2 < … < En …), які називаються енергетичними рівнями атома. Інших значень енергія атома набувати не може.
Другий постулат(рівняння частот). Енергія атома може змінюватись тільки стрибкоподібно – шляхом квантового переходу атома з одного стаціонарного стану в інший (переходу електрона з однієї стаціонарної орбіти на іншу). При переході електрона з енергетичного рівня з більшою енергією Eк на рівень з меншою енергією Еn атом випромінює квант енергії, частота ν якого визначається умовою:
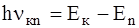 , (1)
, (1)
При квантовому переході в зворотному напрямку, Ек Еn, атом поглинає відповідну кількість енергії. Набір усіх можливих дискретних частот νкn при квантових переходах і визначає лінійчатий спектр випромінювання атома.
Відмітимо, що рівняння частот (1) написано на основі застосування для квантових переходів закону збереження енергії.
При вирішенні питання про те, які саме електронні орбіти в атомі є дозволеними, Бору довелося ввести ще одну додаткову гіпотезу, яку називають умовою квантування (іноді – третім постулатом): орбітальний момент імпульсу електрона на дозволеній (стаціонарній) орбіті повинен бути кратний величині 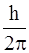 :
:
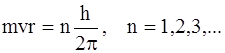 (2)
(2)
де m – маса електрона; v – швидкість його руху по орбіті радіуса r; h – стала Планка.
Дата добавления: 2015-10-06; просмотров: 989;
