Электрохимическая защита
Различают три вида электрохимической защиты: протекторная, катодная и анодная.
Протекторная защита. Защищаемое от коррозии изделие соединяют с металлическим ломом из более электроотрицательного металла (протектора). Это равносильно созданию гальванического элемента, в котором протектор является анодом и будет разрушаться. Например, для защиты подземных сооружений (трубопроводов) на некотором расстоянии от них закапывают протектор (сплавы магния, цинк), присоединив его к сооружению (рис.9).
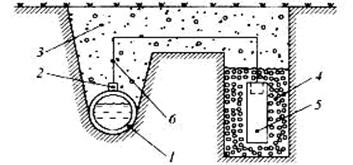
Рис. 9. Схема протекторной защиты: 1-защищаемый трубопровод; 2- стальной наконечник; 3-грунт; 4-засыпка (суспензия бетонита и алебастра); 5-протектор («жертвенный анод – Mg,Zn); 6-стальной провод с изоляцией
Цинковые протекторы применяются с 1825 г., когда Х. Дэви предложил использовать цинк для защиты медной обшивки
деревянных корпусов кораблей. В настоящее время протекторы на основе магниевых сплавов широко используются для защиты корпусов судов от коррозии в морской воде.
Протекторы, играющие роль анода, чаще применяются по сравнению с методами, связанными с использованием внешних источников тока (см. ниже катодная и анодная защита), поскольку протекторы не требуют затрат на оборудование и электроэнергию.
Катодная защита отличается от протекторной тем, что защищаемая конструкция, находящаяся в электролите (почвенная вода), присоединяется к катоду внешнего источника тока. В ту же среду помещают металлолом, который соединяют с анодом внешнего источника тока (рис.10).












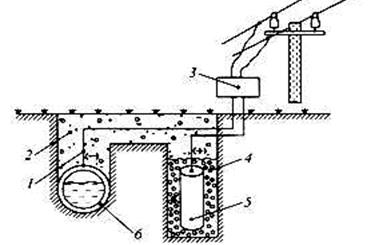
Рис. 10. Схема катодной защиты. 1- провод с изоляцией; 2- грунт; 3-выпрямитель тока; 4- засыпка; 5-вспомогательный анод; 6-защищаемая конструкция (трубопровод)
Металлический лом, являясь анодом, подвергается разрушению, предохраняя от разрушения защищаемую конструкцию. На конструкцию подается отрицательный потенциал и, следовательно,
на ней возможны процессы только восстановления.
Анодная защита используется только для тех металлов, которые 22
при анодной нагрузке способны образовывать на своей поверхности пассивные оксидные или солевые пленки, защищающие металл от коррозии, например, железо в серной кислоте (рис.11).
Б 
I, А 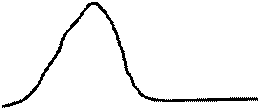
А В С
+Е, В
Рис. 11. АБ-активное растворение; БВ – образование пассивирующей пленки; ВС-пассивная область.
Анодная защита отличается от катодной тем, что защищаемая конструкция, присоединяется к положительному полюсу внешнего источника тока. В ту же среду помещают металлолом, который соединяют с отрицательным полюсом внешнего источника тока (рис. 12).
Из рис. 11 видно, что на поляризационной кривой имеется три характерных участка АБ, БВ и ВС. По мере повышения потенциала анода, на отрезке АБ наблюдается активное растворение металла. Максимум отвечает началу формирования пассивных пленок на поверхности, которые и тормозят растворение металла. Отрезку ВС соответствует пассивная область, когда поверхность полностью перекрыта пассивной пленкой и ток растворения очень мал.
- + 












 | |||||||
 |  |  | |||||

 Б А
Б А
 |  |
Рис. 12. Схема анодной защиты. А – конструкция; Б – металлолом
Поддерживая на защищаемой конструкции потенциал, отвечающий пассивной области поляризационной кривой, мы, таким образом, защищаем ее от коррозии.
Дата добавления: 2015-07-22; просмотров: 6493;
