Условия самопроизвольного протекания процессов
1. Процессы, протекающие в изолированной системе.Подставив в уравнение второго закона термодинамики (26) величину Q из математической записи первого закона термодинамики (2), получаем объединённое выражение:
TdS 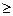 dU + pdV. (38)
dU + pdV. (38)
Учитывая, что энергия и объём изолированной системы есть величины постоянные, то dU = 0 и dV = 0, получаем:
dS 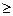 0 (39)
0 (39)
Знак неравенства относится к необратимым процессам.
В изолированной системе самопроизвольно протекают процессы, сопровождающиеся увеличением энтропии. При достижении максимально возможного для данных условий значения энтропии в системе устанавливается состояние равновесия (dS = 0).
Таким образом, изменение энтропии является критерием возможности самопроизвольного протекания химического процесса в изолированной системе:
если dS > 0 – в системе самопроизвольно протекает прямая реакция;
если dS = 0 – система находится в состоянии равновесия;
если dS < 0 – в системе самопроизвольно протекает обратная реакция.
Дата добавления: 2014-12-07; просмотров: 3886;
